题目内容
4.关于反应进行方向的判断,以下说法错误的是( )| A. | 高锰酸钾加热分解是一个熵增的过程 | |
| B. | 能自发进行的化学反应不一定是△H<0、△S<0 | |
| C. | △H<0的化学反应均是自发反应,△S<0的化学反应均不能自发进行 | |
| D. | 反应2Al2O3(s)+3C(s)═2Al(s)+3CO2(g)在常温下不能自发进行,说明该反应△H>0 |
分析 △H-T△S<0的反应可自发进行,结合化学计量数判断△S,结合反应进行方向判断△H,以此来解答.
解答 解:A.高锰酸钾加热分解,由固态生成气体,混乱度增大,则一个熵增的过程,故A正确;
B.△H-T△S<0的反应可自发进行,则可能为△H<0、△S<0或△H<0、△S>0,故B正确;
C.若△H<0、△S<0,高温下不能自发进行,若△H>0、△S<0,低温下不能自发进行,需要由△H-T△S<0判断是否自发进行,故C错误;
D.2Al2O3(s)+3C(s)═2Al(s)+3CO2(g)的△S>0,在常温下不能自发进行,则△H-T•△S>0,则该反应的△H>0,故D正确;
故选C.
点评 本题考查反应热与焓变,为高频考点,把握反应中焓变、熵变的判断及反应进行方向的判断为解答的关键,侧重分析与应用能力的考查,注意综合判据的应用,题目难度不大.

练习册系列答案
相关题目
14.下列化学用语的书写,正确的是( )
| A. | 水分子的结构式: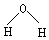 | B. | 氯原子的结构示意图: | ||
| C. | 溴化钠的电子式: | D. | 氮气的电子式: |
15.在一定条件下1molC3H8发生如下反应:①C3H8→C2H4+CH4②C3H8→C3H6+H2如果C3H8的转化率为80%,且混合气体中m(CH4)=m(H2),则下列说法正确的是( )
| A. | 反应后混合气体的平均相对分子质量为35.2 | |
| B. | 两种烯烃物质的量之比,即n(C2H4)/n(C3H6)为1:1 | |
| C. | 将混合气体通入溴的四氯化碳溶液,溶液增重128g | |
| D. | 两种烯烃物质的量之和,即n(C2H4)+n(C3H6)为0.8mol |
12.已知4NH3+5O2═4NO+6H2O,若反应速率分别用v(NH3)、v(O2)、v(NO)、v(H2O)表示,则正确的关系是( )
| A. | $\frac{2}{3}$v(NH3)=v(H2O) | B. | 5v(O2)=6v(H2O) | C. | v(NH3):v(O2)=4:5 | D. | $\frac{5}{4}$v(O2)=v(NO) |
19.向硫酸铜溶液中逐渐滴加氨水,开始形成蓝色沉淀,继续添加氨水,难溶物溶解得到深蓝色的透明溶液.下列对此现象说法正确的是( )
| A. | 反应后溶液中不存在任何沉淀,所以反应前后Cu2+的浓度不变 | |
| B. | 在[Cu(NH3)4]2+离子中,Cu2+是配位原子,NH3是配体 | |
| C. | 在[Cu(NH3)4]2+离子中,Cu2+给出孤对电子,NH3提供空轨道 | |
| D. | 沉淀溶解后,将会生成深蓝色的配合离子[Cu(NH3)4]2+ |
9.有机物甲、乙的结构如图所示.下列说法错误的是( )


| A. | 甲、乙互为同分异构体 | |
| B. | 甲、乙都能与溴的单质发生加成反应 | |
| C. | 甲、乙都能与金属钠反应生成氢气 | |
| D. | 一定条件下,甲、乙均能发生取代反应 |
5. 常温下,用0.10mol•L-1的NaOH溶液分别滴定体积均为50.00mL、浓度均为0.05mol•L-1的HClO、HF两种溶液,其滴定曲线如图所示.下列说法正确的是( )
常温下,用0.10mol•L-1的NaOH溶液分别滴定体积均为50.00mL、浓度均为0.05mol•L-1的HClO、HF两种溶液,其滴定曲线如图所示.下列说法正确的是( )
 常温下,用0.10mol•L-1的NaOH溶液分别滴定体积均为50.00mL、浓度均为0.05mol•L-1的HClO、HF两种溶液,其滴定曲线如图所示.下列说法正确的是( )
常温下,用0.10mol•L-1的NaOH溶液分别滴定体积均为50.00mL、浓度均为0.05mol•L-1的HClO、HF两种溶液,其滴定曲线如图所示.下列说法正确的是( )| A. | HClO的酸性比HF强 | |
| B. | V(NaOH溶液)=0 mL 时,对应溶液中:c(ClO-)=c(F-) | |
| C. | V(NaOH溶液)=12.50 mL 时,对应溶液中:c(ClO-)>c(F-) | |
| D. | V(NaOH溶液)=25.00mL时,对应溶液中:c(ClO-)<c(F-) |
3.通常情况下,既能用浓硫酸干燥,又能用碱石灰干燥的是( )
| A. | NH3 | B. | Cl2 | C. | CO | D. | HCl |

 ;加聚反应.
;加聚反应.