题目内容
(9分)元素A~D是元素周期表中短周期的四种元素,请根据表中信息回答下列问题。
(1)上表中与A属于同一周期的元素是 (填元素名称),写出D离子结构示意图 。
(2)D和B形成的化合物的化学式为 。
写出A单质与水反应的离子方程式 。
(3)对B、C的单质或化合物描述正确的是 。
a.C元素的最高正价为+7 b.常温、常压下C单质性质稳定
c.B的氧化物只有两种 d.C单质分子中含有18个电子
(4)从海水中提取D的单质可按如下步骤进行:①把贝壳制成石灰乳;②向引入的海水中加入石灰乳,沉降、洗涤、过滤沉淀物;③将沉淀物与盐酸反应,结晶、过滤、干燥;④电解得到产物。以上提取D的单质的过程中,没有涉及的化学反应类型是
a.分解反应 b.化合反应 c.复分解反应 d.置换反应
(1)镁 (1分)  (1分)
(1分)
(2)Mg3N2 (1分) 2Na + 2H2O = 2Na+ +2OH- + H2↑ (2分)
(3)d (2分) (4)d (2分)
解析先从表格里提炼信息:单质在空气中燃烧生成淡黄色物质的,高中阶段只有金属钠,再结合过氧化钠与水或二氧化碳反应生成氧气的事实,可以确定A为Na。由氢化物极易溶水且水溶液为碱性,可知B为N。C的-1价阴离子与氖相同,即C的核电荷数为9,是F。D的+2价阳离子核外电子排布与氖原子相同,可知D的核电荷数为12,是Mg。
(1) 与Na同周期的只有Mg,属于第三周期。Mg2+核外电子共12个,正好填满两个电子层,结构为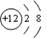 。
。
(2) Mg和N形成化合物,联想到把点燃镁条深入氮气的实验的产物,为Mg3N2。Na与水反应的离子方程式是书上要求重点记忆的2Na + 2H2O = 2Na+ +2OH- + H2↑。
(3) a.容易把F和其他卤素记混,但要特别记住F只有-1价和0价,故此项错误。
b.F2作为有强非金属性的元素的单质,化学性质活泼,性质不稳定,故此项错误。
c.Na的氧化物有氧化钠、过氧化钠和超氧化钠三种,故此项错误。
d. F2两个氟原子通过一个共价键相连,共18个电子,故此项正确。
(4) 把贝壳制成石灰乳涉及两个反应:
1.CaCO3==CaO+CO2↑(条件为高温,这是分解反应)
2.CaO+H2O= =Ca(OH)2(这是化合反应)
向引入的海水中加入石灰乳主要是一个反应:
MgCl2+Ca(OH)2==Mg(OH)2↓+CaCl2(这是复分解反应)
将沉淀物与盐酸反应,结晶、过滤、干燥中有一个反应:
Mg(OH)2+2HCl==MgCl2+2H2O(这是复分解反应)
电解产物就是电解氯化镁:
MgCl2(熔融)==Mg+Cl2↑(条件是电解,这是分解反应)
所以整个过程没有置换反应。

 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案元素A~D是元素周期表中短周期的四种元素,请根据表中的信息回答下列问题。
| 元素 | A | B | C | D |
| 物质或结构信息 | 单质制成的的高压灯,发出的黄光透雾力强、射程远。 | 工业上通过分离液态空气获得其单质。原子的最外层未达到稳定结构 | 单质常温、常压下是气体,原子的L层有一个未成对的 | +2价阳离子的核外电子排布与氖原子相同。 |
(1)上表中与A属于同一周期的元素是_____________(写元素符号) ,写出D离子的电子排布式______________________。
(2)D和C形成的化合物属于_________晶体 。写出C单质与水反应的化学方程式_________________________ 。
(3)对元素B的单质或化合物描述正确的是_________。
a.B元素的最高正价为+6 b.常温、常压下单质难溶于水
c.单质分子中含有18个电子 d.在一定条件下镁条能与单质B反应
(4)A和D两元素金属性较强的是(写元素符号)__ ___。 写出能证明该结论的一个实验事实___________ _____。
元素A~D是元素周期表中短周期的四种元素,请根据表中的信息回答下列问题。
| 元素 | A | B | C | D |
| 物质或结构信息 | 单质制成的的高压灯,发出的黄光透雾力强、射程远。 | 工业上通过分离液态空气获得其单质。原子的最外层未达到稳定结构 | 单质常温、常压下是气体,原子的L层有一个未成对的 | +2价阳离子的核外电子排布与氖原子相同。 |
(1)上表中与A属于同一周期的元素是_____________(写元素符号) ,写出D离子的电子排布式______________________。
(2)D和C形成的化合物属于_________晶体 。写出C单质与水反应的化学方程式_________________________ 。
(3)对元素B的单质或化合物描述正确的是_________。
a.B元素的最高正价为+6 b.常温、常压下单质难溶于水
c.单质分子中含有18个电子 d.在一定条件下镁条能与单质B反应
(4)A和D两元素金属性较强的是(写元素符号)__ ___。 写出能证明该结论的一个实验事实___________ _____。

