题目内容
13.制取过氧乙酸反应原理为H2O2++CH3COOH$\stackrel{浓H_{2}SO_{4}}{→}$CH3COOOH(过氧乙酸)+H2O,现称取5.0g用上述方法制取的过氧乙酸试样(液体),稀释至100mL备用.取上述稀释后过氧乙酸试样5.0mL,用0.01mol•L-1KMnO4溶液以除去其中的H2O2,随即加入10%KI溶液10mL,摇匀,(化学方程式CH3COOOH+2KI═CH3COOK+I2+KOH),再将0.05mol•L-1 Na2S2O3标准溶液加入到上述混合溶液中(化学反应方程式为:I2+2Na2S2O3═2NaI+Na2S4O6),消耗Na2S2O3标准溶液的总体积为20mL.试计算确定原试样中过氧乙酸的质量分数为15.2%.分析 根据CH3COOOH+2H++2I-=I2+CH3COOH+H2O及I2+2S2O32-=2I-+S4O62-两个化学方程式,可以得关系式如下:CH3COOOH~I2~2Na2S2O3,据此计算稀释后5mL反应中n(CH3COOOH),进而计算原试样中过氧乙酸的质量分数.
解答 解:根据CH3COOOH+2H++2I-=I2+CH3COOH+H2O及I2+2S2O32-=2I-+S4O62-两个化学方程式,可以得关系式如下:CH3COOOH~I2~2Na2S2O3,由关系式可知,n(CH3COOOH)=$\frac{1}{2}$n(Na2S2O3)=$\frac{1}{2}$×0.05mol/L×0.02L=5×10-4mol,故原样品中w(CH3COOOH)=$\frac{5×1{0}^{-4}mol×76g/mol}{5g×\frac{5mL}{100mL}}$×100%=15.2%,
故答案为:15.2%.
点评 本题考查氧化还原反应滴定、实验原理的分析和多步反应关系的计算等,难度中等,注意利用关系式进行计算,为易错点,学生容易忽略滴定中所取溶液的体积,按稀释后溶液体积计算,导致错误答案.

练习册系列答案
相关题目
1.C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2,下列做法不能加快化学反应速率的是( )
| A. | 增大氧气浓度 | B. | 升高反应温度 | C. | 增大木炭的量 | D. | 将炭磨成炭粉 |
2.某中学化学兴趣小组为了测定某矿山石灰石中碳酸钙的质量分数,取石灰石样品与足量的10%的稀盐酸在烧杯中反应(假设石灰石样品中杂质不与稀盐酸反应也不溶于水).有关实验数据如下表:
请计算(写出计算过程):
(1)该石灰石中碳酸钙的质量分数;
(2)参加反应10%的盐酸的质量.
| 反应前 | 反应后 | ||
| 实验 数据 | 烧杯和稀盐酸的质量 | 石灰石样品的质量 | 烧杯和其中混合物的质量 |
| 134.4 g | 10 g | 141.1 g | |
(1)该石灰石中碳酸钙的质量分数;
(2)参加反应10%的盐酸的质量.
 金属镍及其化合物在合金材料以及催化剂等方面应用广泛.
金属镍及其化合物在合金材料以及催化剂等方面应用广泛. 、④HCHO,其中碳原子采取sp2杂化的分子有①③④(填物质序号),HCHO分子的立体结构为平面三角形.
、④HCHO,其中碳原子采取sp2杂化的分子有①③④(填物质序号),HCHO分子的立体结构为平面三角形.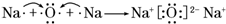 .A、B两种元素还可以形成A2B2型化合物,写出该化合物的电子式
.A、B两种元素还可以形成A2B2型化合物,写出该化合物的电子式 .
.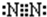 ;
; ;
;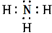 .
.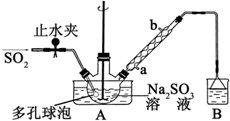 次硫酸氢钠甲醛(NaHSO2•HCHO•2H2O)俗称吊白块,不稳定,120℃时会分解.在印染、医药以及原子能工业中有广泛应用.以Na2SO3、SO2、HCHO和锌粉为原料制备次硫酸氢钠甲醛的实验步骤如图:
次硫酸氢钠甲醛(NaHSO2•HCHO•2H2O)俗称吊白块,不稳定,120℃时会分解.在印染、医药以及原子能工业中有广泛应用.以Na2SO3、SO2、HCHO和锌粉为原料制备次硫酸氢钠甲醛的实验步骤如图: