题目内容
5.X、Y、Z、M、N为短周期的五种主族元素,其中X、Z同主族,Y、Z同周期,M与X、Y既不同族,也不同周期.X原子最外层电子数是核外电子层数的三倍,Y的最高化合价与其最低化合价的代数和等于6.N是短周期主族元素中原子半径最大的非金属元素.(1)请写出下列元素的元素符号:XO,YCl,MH.
(2)请写出下列反应的离子方程式:N单质与NaOH溶液反应:Si+2OH-+H2O=SiO32-+2H2↑.
(3)Y与Z相比,非金属性较强的元素是Cl(填元素符号),可以证明该结论的实验是(用离子方程式表示)Cl2+S2-=2Cl-+S↓.
分析 X、Y、Z、M、N为短周期的五种主族元素,X原子最外层电子数是核外电子层数的三倍,原子只能有2个电子层,最外层电子数为6,则X为O元素;X、Z同主族,则Z为S元素;Y的最高化合价与其最低化合价的代数和等于6,处于ⅦA族,且Y、Z同周期,则Y为Cl;N是短周期主族元素中原子半径最大的非金属元素,则N为Si;M与X、Y既不同族,也不同周期,则M为H元素,据此解答.
解答 解:X、Y、Z、M、N为短周期的五种主族元素,X原子最外层电子数是核外电子层数的三倍,原子只能有2个电子层,最外层电子数为6,则X为O元素;X、Z同主族,则Z为S元素;Y的最高化合价与其最低化合价的代数和等于6,处于ⅦA族,且Y、Z同周期,则Y为Cl;N是短周期主族元素中原子半径最大的非金属元素,则N为Si;M与X、Y既不同族,也不同周期,则M为H元素.
(1)由上述分析可知,X为O元素,Y为Cl元素,M为H元素,故答案为:O;Cl;H;
(2)N单质与NaOH溶液反应离子方程式为:Si+2OH-+H2O=SiO32-+2H2↑,故答案为:Si+2OH-+H2O=SiO32-+2H2↑;
(3)S与Cl相比,非金属性较强的元素是Cl,可以证明该结论的实验是(用离子方程式表示):Cl2+S2-=2Cl-+S↓,故答案为:Cl;Cl2+S2-=2Cl-+S↓.
点评 本题考查结构性质位置关系综合应用,难度不大,注意元素金属性与非金属性强弱比较实验事实.

练习册系列答案
相关题目
13. 6种相邻短周期主族元素的相对位置如表,M元素原子核外电子数是Y元素原子核外电子数的2倍,W元素原子的次外层电子数是最外层电子数的2倍.用化学用语回答下列问题:
6种相邻短周期主族元素的相对位置如表,M元素原子核外电子数是Y元素原子核外电子数的2倍,W元素原子的次外层电子数是最外层电子数的2倍.用化学用语回答下列问题:
(1)Y在周期表中的位置是第二周期ⅥA族.
(2)X、Y、Z三种元素的原子半径由大到小的顺序是r(N)>r(O)>r(F).
(3)W、M、Q三种元素最高价氧化物对应的水化物中,酸性由强到弱的顺序是HClO4>H2SO4>H2SiO3.
(4)X的含10个电子的气态氢化物甲是一种重要的化工原料.甲可以与X的最高价氧化物对应的水化物溶液反应生成盐乙,乙溶液中的离子浓度由大到小的顺序是c(NO3-)>c(NH4+)>c(H+)>c(OH-).X的含18个电子的气态氢化物丙可与空气构成一种环保型碱性燃料电池,电池工作时丙发生的电极反应式是N2H4-4e-+4OH-═N2+4H2O.
(5)工业上用如图所示装置电解Q元素的钠盐溶液丁,获得一种含Q元素的消毒剂丙.该反应的离子方程式是Cl-+H2O $\frac{\underline{\;电解\;}}{\;}$ClO-+H2↑.丙的电子式 .
.
(6)洁厕灵的主要成分是HCl.下列关于卤化氢的性质比较中错误的是AC
A.酸性:HF>HCl>HBr>HI B.键能:H-F>H-Cl>H-Br>H-I
C.沸点:HF<HCl<HBr<HI D.还原性:HF<HCl<HBr<HI.
 6种相邻短周期主族元素的相对位置如表,M元素原子核外电子数是Y元素原子核外电子数的2倍,W元素原子的次外层电子数是最外层电子数的2倍.用化学用语回答下列问题:
6种相邻短周期主族元素的相对位置如表,M元素原子核外电子数是Y元素原子核外电子数的2倍,W元素原子的次外层电子数是最外层电子数的2倍.用化学用语回答下列问题:| X | Y | Z | |
| W | M | Q |
(2)X、Y、Z三种元素的原子半径由大到小的顺序是r(N)>r(O)>r(F).
(3)W、M、Q三种元素最高价氧化物对应的水化物中,酸性由强到弱的顺序是HClO4>H2SO4>H2SiO3.
(4)X的含10个电子的气态氢化物甲是一种重要的化工原料.甲可以与X的最高价氧化物对应的水化物溶液反应生成盐乙,乙溶液中的离子浓度由大到小的顺序是c(NO3-)>c(NH4+)>c(H+)>c(OH-).X的含18个电子的气态氢化物丙可与空气构成一种环保型碱性燃料电池,电池工作时丙发生的电极反应式是N2H4-4e-+4OH-═N2+4H2O.
(5)工业上用如图所示装置电解Q元素的钠盐溶液丁,获得一种含Q元素的消毒剂丙.该反应的离子方程式是Cl-+H2O $\frac{\underline{\;电解\;}}{\;}$ClO-+H2↑.丙的电子式
 .
.(6)洁厕灵的主要成分是HCl.下列关于卤化氢的性质比较中错误的是AC
A.酸性:HF>HCl>HBr>HI B.键能:H-F>H-Cl>H-Br>H-I
C.沸点:HF<HCl<HBr<HI D.还原性:HF<HCl<HBr<HI.
17.2014年是门捷列夫诞辰180周年.下列事实不能用元素周期律解释的只有( )
| A. | 碱性:KOH>NaOH | B. | 元素的金属性:Mg>Al | ||
| C. | 酸性:HClO4>H2SO4 | D. | 相对分子质量:Ar>K |
14.如图所示,试管中盛有已检出部分离子的某溶液,下列推理正确的是( )


| A. | 向该溶液中加入Mg有H2逸出 | |
| B. | 向该溶液中加入少量FeCl2,其离子反应方程式为:2NO3-+6I-+4H2O | |
| C. | 该溶液还可能大量存在MnO4-、ClO- | |
| D. | 向该溶液中逐滴加入Na2CO3溶液至过量,既有气体逸出又有沉淀生成 |

 ;粒子E的名称是水合氢离子;粒子F对应的元素在周期表中的位置是第三周期、ⅢA族.
;粒子E的名称是水合氢离子;粒子F对应的元素在周期表中的位置是第三周期、ⅢA族.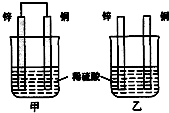 (1)已知:△H>0为吸热反应、△H<0为放热反应.实事证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是C.
(1)已知:△H>0为吸热反应、△H<0为放热反应.实事证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是C.