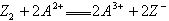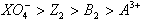��Ŀ����
��֪�����£�����Һ�з������·�Ӧ����16H++10Z��+2XO4��=2X2++5Z2+8H2O����2A2++B2=2A3��+2B������2B��+Z2=B2+2Z���ɴ��ƶ�����˵���������( )��
| A����ӦZ2+2A2+=2A3++2Z�����Խ��� |
| B��ZԪ���ڢٷ�Ӧ�б��������ڢ۷�Ӧ�б���ԭ |
| C����ԭ����ǿ������˳����Z����B����A2+��X2+ |
| D����������ǿ������˳����XO4����Z2��B2��A3+ |
C
���������������������ʽ�� 16H++10Z��+2XO4��=2X2++5Z2+8H2O����������XO4��������������Z2����������XO4����>Z2; ����B2�����������Դ����������� A3���������ԡ�����Z2�����������Դ�����������B2��������, Z2����ԭ������A��B��D��ȷ��ͬ���ɷ�����ԭ����ǿ������˳���ǣ�A2+��B����Z����X2+��C����

��ϰ��ϵ�д�
�����Ŀ