题目内容
下列关于金属的性质的说法正确的是( )
| A、金属钠长期暴露在空气中,表面变暗最终生成白色固体氧化钠 |
| B、钠着火时,我们可以用煤油扑灭 |
| C、金属原子最外层电子越少,其还原性越强 |
| D、铝表面有致密的氧化膜,所以铝在空气中能稳定存在而且应用非常广泛 |
考点:钠的化学性质,铝的化学性质
专题:
分析:A.钠长期放置在空气中,发生一系列变化最终变为碳酸钠;
B.煤油是易燃物;
C.金属性强弱与失去电子难易有关,与最外层电子数多少无关;
D.铝在空气中稳定存在的原因是在常温下Al与氧气反应生成氧化铝致密的保护膜.
B.煤油是易燃物;
C.金属性强弱与失去电子难易有关,与最外层电子数多少无关;
D.铝在空气中稳定存在的原因是在常温下Al与氧气反应生成氧化铝致密的保护膜.
解答:
解:A.钠长期放置在空气中,先和氧气反应生成氧化钠、氧化钠和水反应生成氢氧化钠,氢氧化钠潮解,氢氧化钠溶液和二氧化碳反应生成十水碳酸钠,十水碳酸钠风化得到碳酸钠,所以钠发生一系列变化最终变为碳酸钠,故A错误;
B.煤油是易燃物,不能用来灭火,故B错误;
C.金属性强弱与失去电子难易有关,与最外层电子数多少无关,如Al原子最外层电子数比Na原子多,但Na的金属性强,失去电子的能力强,故C错误;
D.铝在空气中稳定存在的原因是在常温下Al与氧气反应生成氧化铝致密的保护膜,故D正确;
故选D.
B.煤油是易燃物,不能用来灭火,故B错误;
C.金属性强弱与失去电子难易有关,与最外层电子数多少无关,如Al原子最外层电子数比Na原子多,但Na的金属性强,失去电子的能力强,故C错误;
D.铝在空气中稳定存在的原因是在常温下Al与氧气反应生成氧化铝致密的保护膜,故D正确;
故选D.
点评:本题考查了钠及其氧化物的性质,明确物质的性质是解本题关键,再结合基本概念来分析解答,题目难度不大.

练习册系列答案
 浙大优学小学年级衔接捷径浙江大学出版社系列答案
浙大优学小学年级衔接捷径浙江大学出版社系列答案
相关题目
从我国西部开采的天然气,通过西气东输工程供给江苏.天然气的主要成分是( )
| A、甲烷 | B、氢气 |
| C、一氧化碳 | D、乙烯 |
在25℃、101KPa下,1g甲醇燃烧生成CO2和液态水时放热22.68KJ,下列热化学方程正确的是( )
A、CH3OH(l)+
| ||
| B、2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(l)△H=-1452KJ/mol | ||
C、CH3OH(l)+
| ||
| D、2CH3OH(l)+3O2(g)=2CO2(g)+4H2O(g)△H=-1452KJ/mol |
下列说法正确的是( )
| A、物质发生化学变化都伴随着能量变化 |
| B、伴有能量变化的物质变化都是化学变化 |
| C、在一个确定的化学反应关系中,反应物的总能量与生成物的总能量一定相等 |
| D、在一个确定的化学反应关系中,反应物的总能量总是高于生成物的总能量 |
定温时将pH=2的盐酸和醋酸分别稀释到pH=3时,所稀释时用水的体积前者与后者的关系是( )
| A、大于 | B、小于 |
| C、等于 | D、不能确定 |
 锌电池用锌作负极的电池生活中随处可见,如锌锰干电池、锌锰碱性电池、锌空电池等.
锌电池用锌作负极的电池生活中随处可见,如锌锰干电池、锌锰碱性电池、锌空电池等.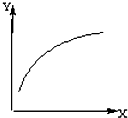 在密闭容器中加入A、B两种物质,在一定条件下反应:2A(s)+B(g)?2C(g) (△H<0).达到平衡后,改变一个条件(X),下列量(Y)的变化一定符合图中曲线的是( )
在密闭容器中加入A、B两种物质,在一定条件下反应:2A(s)+B(g)?2C(g) (△H<0).达到平衡后,改变一个条件(X),下列量(Y)的变化一定符合图中曲线的是( )