题目内容
反应N2+3H2 2NH3刚开始时,N2的浓度为3 mol/L,H2的浓度为5 mol/L,3 min后测得NH3浓度为0.6 mol/L,则此时间内,下列反应速率表示正确的是
2NH3刚开始时,N2的浓度为3 mol/L,H2的浓度为5 mol/L,3 min后测得NH3浓度为0.6 mol/L,则此时间内,下列反应速率表示正确的是
A.v(NH3)=0.2 mol/(L·s) B.v(N2)=1.0 mol/(L·min)
C.v(H2)=1.67 mol/(L·min) D.v(H2)=0.3 mol/(L·min)
【答案】
D
【解析】
试题分析: N2
+ 3H2  2NH3
2NH3
起始浓度:3 mol/L 5 mol/L 0
转化浓度:0.3 mol/L 0.9 mol/L 0.6 mol/L
平衡浓度:2.7 mol/L 4.1 mol/L 0.6 mol/L
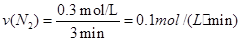
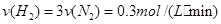
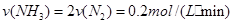
因此选D。
考点:考查化学反应速率。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
 2NH3.在10s内N2的浓度由5mol/L降至4mol/L下列说法正确的是( )
2NH3.在10s内N2的浓度由5mol/L降至4mol/L下列说法正确的是( ) 2NH3 下列不是该反应达到平衡状态标志的是( )
2NH3 下列不是该反应达到平衡状态标志的是( ) 2NH3,下列有关推断正确的是( )
2NH3,下列有关推断正确的是( )
 2NH3的△H
2NH3的△H 2NH3,下列选项不能作为反应达到平衡状态标志的是( )
2NH3,下列选项不能作为反应达到平衡状态标志的是( )