题目内容
| |||||||||||
解析:
(1) |
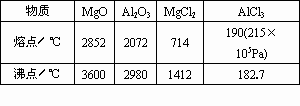
因为MgO的熔点远高于MgCl2,故电解熔融MgO将需要更高的温度,不便于操作.观察表中数据可见,AlCl3易升华,熔、沸点低,故属于分子晶体,不存在离子,不能被电解. |
(2) |
将两种晶体加热到熔化状态,MgCl2能导电,AlCl3不能导电,故确证MgCl2为离子晶体,AlCl3为分子晶体.要注意由于MgCl2、AlCl3溶于水都能电离,不能用它们的溶液作导电性实验来证明所属晶体类型. |

 课课练江苏系列答案
课课练江苏系列答案 名牌中学课时作业系列答案
名牌中学课时作业系列答案 明天教育课时特训系列答案
明天教育课时特训系列答案已知有关物质的熔、沸点数据如表:
|
下图是某工厂对海水资源进行综合利用的示意图.
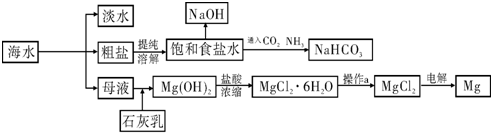
请回答下列问题:
(1)请列举一种海水淡化的方法
(2)工业上常用离子交换膜电解槽生产NaOH,电解过程中大量通过离子交换膜的离子是
(3)侯氏制碱法中首先向饱和食盐水中通入CO2和NH3制得NaHCO3,先通入
(填化学式),理由是
(4)镁是一种用途很广泛的金属材料,目前世界上60%的镁从海水中提取.已知有关物质的熔沸点数据如下:
| MgO | MgCl2 | |
| 熔点/℃ | 2852 | 714 |
| 沸点/℃ | 3600 | 1412 |
| 物质 | MgO | Al2O3 | MgCl2 | AlCl3 |
| 熔点(℃) | 2850 | 2072 | 714 | 190(2.5×105Pa) |
| 沸点(℃) | 3600 | 2980 | 1412 | 182.7 |
工业上常用电解熔融的MgCl2方法生产金属镁,电解Al2O3和冰晶石的熔融体的方法生产铝,为什么不用电解MgO的方法生产镁?也不用电解氯化铝的方法生产铝?
物质 | MgO | Al2O3 | MgCl2 | AlCl3 |
熔点/℃ | 2852 | 2072 | 714 | 190(2.5×105 Pa) |
沸点/℃ | 3600 | 2980 | 1420 | 182.7 |
请参考上述数据,填空和回答下列问题。
(1)工业上用电解熔融MgCl2的方法生产金属镁,电解Al2O3与冰晶石熔融混合物的方法生产铝。为什么不用电解MgO的方法生产镁,也不用电解AlCl3的方法生产铝?
(2)设计可靠的实验,证明MgCl2、AlCl3所属的晶体类型,其实验方法是:______________________________。
| MgO | Al2O3 | MgCl2 | AlCl3 |
熔点/ ℃ | 2 852 | 2 072 | 714 | 190(2.5×105Pa) |
沸点/ ℃ | 3 600 | 2 980 | 1 412 | 182.7 |
请参考上述数据完成下列问题:
(1)工业上常用电解熔融MgCl2的方法生产金属镁,电解Al2O3与冰晶石熔融混合物的方法生产铝。为什么不用电解MgO的方法生产镁,也不用电解AlCl3的方法生产铝?
(2)设计可靠的实验证明MgCl2、AlCl3所属的晶体类型,其实验方法是_________________
_____________________________________________________________________。