题目内容
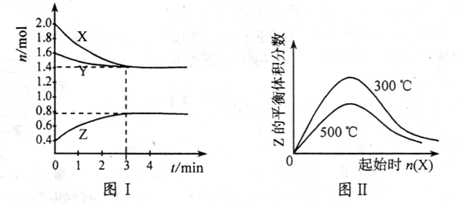
T0C时,在2L密闭容器中,X、Y、Z三种气体的物质的量随时间变化如下图I所示;若起始时加入一定量的Y,在不同温度下改变X的量时Z的体积分数变化情况如图II所示.则下列结论正确的是( )
A.该反应的化学方程式为:2X(g)+Y(g)?2Z(g)
B.反应进行的前3min内,用X表示的平均反应速率
 (X)═0.067mol/
(X)═0.067mol/C.由图II可知,其他条件不变,增大X的量时Y的转化率先增大后减小
D.其他条件不变,升髙温度,平衡逆向移动
B、根据一定时间之内X的浓度变化来计算X的反应速率;
C、其他条件不变,增大X的量时Y的转化率逐渐增大;
D、由图II可知,温度升高Z的体积分数降低,说明升高温度平衡向逆反应方向移动,则正反应放热.
解答:解:A、图Ⅰ中X、Y的物质的量逐渐减小,应为反应物,Z的物质的量逐渐增多,应为生成物,根据反应速率等于化学计量数之比等于物质的量的变化量之比,
则有v(X):v(Y):V(z)=0.6mol:0.2mol:0.4mol=3:1:2,所以方程式为3X(g)+Y(g)
 2Z(g),故A错误;
2Z(g),故A错误;B、反应进行的前3min内,用X表示的平均反应速率
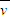 (X)═
(X)═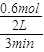 0.1mol/(L?min),故B错误;
0.1mol/(L?min),故B错误;C、其他条件不变时,增大一种反应物的量,另一种反应物的转化率会增大,故C错误;
D、由图II可知,温度升高Z的体积分数降低,说明升高温度平衡向逆反应方向移动,故D正确.
故选D.
点评:本题考查化学平衡图象题,本题难度不大,做题注意C项易错.

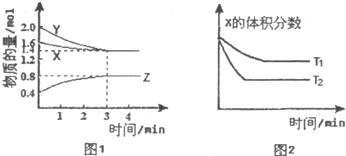
| A、容器中发生的反应可表示为:3X(g)+Y(g)?2Z(g) | B、3min内,用Y表示的反应速率v(Y)=0.2mol/(L?min) | C、保持其他条件不变,升髙温度,化学平衡常数K增大 | D、保持其他条件不变,平衡后,增大体系压强,正反应速率增大,逆反应速率减小 |
铁元素是重要的金属元素,单质铁在工业和生活中使用得最为广泛。铁还有很多重要的化合物及其化学反应。如铁与水反应:3Fe(s)+4H2O(g)=Fe3O4(s)+4H2(g) △H
(1)上述反应的平衡常数表达式K=_______。
(2) 已知:①3Fe(s)+2O2(g)=Fe3O4(s) △H1=-1118.4kJ/mol
②2H2(g)+O2(g)=2H2O(g) △H2=-483.8kJ/mol
③2H2(g)+O2(g)=2H2O(l) △H3=-571.8kJ/mol
则△H=_______。
(3)在t0C时,该反应的平衡常数K=16,在2L恒温恒容密闭容器甲和乙中,分别按下表所示加入物质,反应经过一段时间后达到平衡。
|
|
Fe |
H2O(g) |
Fe3O4 |
H2 |
|
甲/mol |
1.0 |
1.0 |
1.0 |
1.0 |
|
乙/mol |
1.0 |
1.5 |
1.0 |
1.0 |
①甲容器中H2O的平衡转化率为_______ (结果保留一位小数)。
②下列说法正确的是_______ (填编号)
A.若容器压强恒定,则反应达到平衡状态
B.若容器内气体密度恒定,则反应达到平衡状态
C.甲容器中H2O的平衡转化率大于乙容器中H2O的平衡转化率
D.增加Fe3O4就能提高H2O的转化率
(4)若将(3)中装置改为恒容绝热(不与外界交换能量)装置,按下表充入起始物质,起始时与平衡后的各物质的量见表:
|
|
Fe |
H2O(g) |
Fe3O4 |
H2 |
|
起始/mol |
3.0 |
4.0 |
0 |
0 |
|
平衡/mol |
m |
n |
p |
q |
若在达平衡后的装置中继续加入A、B、C三种状况下的各物质,见表:
|
|
Fe |
H2O(g) |
Fe3O4 |
H2 |
|
A/mol |
3.0 |
4.0 |
0 |
0 |
|
B/mol |
0 |
0 |
1 |
4 |
|
C/mol |
m |
n |
p |
q |
当上述可逆反应再一次达到平衡状态后,上述各装置中H2的百分含量按由大到小的顺序排列的关系是
________(用A、B、C表示)。
(5)已知Fe(OH)3的Ksp=2.79×10-39,而FeCl3溶液总是显示较强的酸性,若某FeCl3溶液的pH为3,则该溶液中c(Fe3+)=________mol • L-1 (结果保留3位有效数字)