题目内容
将NaOH、Na2CO3、NaHCO3、CaO组成的混合物18.6g溶于足量水中,充分搅拌一段时间后,测得Ca2+、A.10.6g B.5.3g C.7.8g D.2.65g
B
解析:反应前混合物18.6 g,反应后混合物19.5g,反应前后质量差即为CaO所吸收的水的质量:19.5g-18.6g=0.9g
CaO+H2O====Ca(OH)2
1mol 18 g
xmol 0.9 g
x=0.05 mol
即反应前CaO的质量:0.05mol×56g/mol=2.8g
反应后的混合物为NaOH和CaCO3二者构成
其中CaCO3:0.05mol×100g/mol=5g
NaOH:19.5 g-5 g=14.5 g
设 NaOH—amol Na2CO3—6mol NaHCO3—c mol
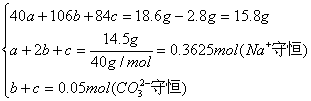
解出b=0.05mol从而,m Na2CO3=106g·mol-×0.05 mol=5.3 g

练习册系列答案
相关题目
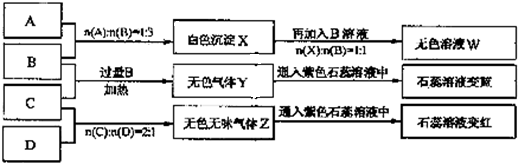
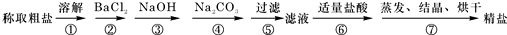
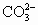 ,
, 均已转化为沉淀.若将反应器中的水分蒸干,最后得到白色固体物质共19.5g.则原混合物中Na2CO3的质量是
均已转化为沉淀.若将反应器中的水分蒸干,最后得到白色固体物质共19.5g.则原混合物中Na2CO3的质量是