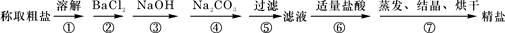题目内容
(1)为除去粗盐中的Ca2+、Mg2+、Fe3+、SO42-以及泥沙等杂质,某同学设计了一种制备精盐的实验方案,步骤如下(用于沉淀的试剂稍过量):
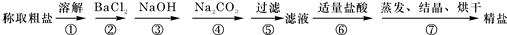
①第5步实验操作需要烧杯、
②步骤2中,判断加入BaCl2已过量的方法是:
③除杂试剂BaCl2、NaOH、Na2CO3加入的顺序必须满足
④若先用盐酸调pH值再过滤,将对实验结果产生影响,其原因是
(2)为检验粗盐溶液中Cl-、SO42-请根据内容填空:
①首先检验
②将所得混合物过滤,然后在溶液中加入试剂
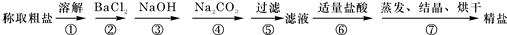
①第5步实验操作需要烧杯、
玻璃棒
玻璃棒
、漏斗
漏斗
玻璃仪器.②步骤2中,判断加入BaCl2已过量的方法是:
取第②步后的上层清液(或取少量上层清液于试管中),再滴入适量BaCl2溶液,若溶液未变浑浊,则表明BaCl2已过量
取第②步后的上层清液(或取少量上层清液于试管中),再滴入适量BaCl2溶液,若溶液未变浑浊,则表明BaCl2已过量
.③除杂试剂BaCl2、NaOH、Na2CO3加入的顺序必须满足
在氢氧化钠和氯化钡试剂加入后再加入碳酸钠;
在氢氧化钠和氯化钡试剂加入后再加入碳酸钠;
.④若先用盐酸调pH值再过滤,将对实验结果产生影响,其原因是
在此酸度条件下,会有部分沉淀溶解,从而影响制得精盐的纯度;
在此酸度条件下,会有部分沉淀溶解,从而影响制得精盐的纯度;
.(2)为检验粗盐溶液中Cl-、SO42-请根据内容填空:
①首先检验
SO42-
SO42-
离子,应先加入过量的Ba(NO3)2
Ba(NO3)2
.②将所得混合物过滤,然后在溶液中加入试剂
硝酸酸化的硝酸银
硝酸酸化的硝酸银
检验另一离子.分析:(1)①根据过滤操作要求分析;依据过滤实验用到的仪器来回答;
②根据钡离子能和硫酸根之间反应生成硫酸钡沉淀来检验氯化钡是否过量;
③碳酸钠可以将钙离子以及过量的钡离子沉淀下来;除镁离子用氢氧化钠,除钙离子用碳酸钠,除硫酸根离子用氯化钡,所加试剂要过量,为了将多余的杂质除掉,碳酸钠必须放在氯化钡的后面;
④氢氧化镁沉淀、碳酸钙沉淀均会和盐酸反应;
(2)氯化银、硫酸钡均是不溶于稀硝酸的白色沉淀;在检验氯离子时,是加入硝酸银出现白色沉淀,证明氯离子的存在;但是硫酸银是微溶于水的,量多了也就变成沉淀了,所以要先检验硫酸根离子,再检验氯离子.
②根据钡离子能和硫酸根之间反应生成硫酸钡沉淀来检验氯化钡是否过量;
③碳酸钠可以将钙离子以及过量的钡离子沉淀下来;除镁离子用氢氧化钠,除钙离子用碳酸钠,除硫酸根离子用氯化钡,所加试剂要过量,为了将多余的杂质除掉,碳酸钠必须放在氯化钡的后面;
④氢氧化镁沉淀、碳酸钙沉淀均会和盐酸反应;
(2)氯化银、硫酸钡均是不溶于稀硝酸的白色沉淀;在检验氯离子时,是加入硝酸银出现白色沉淀,证明氯离子的存在;但是硫酸银是微溶于水的,量多了也就变成沉淀了,所以要先检验硫酸根离子,再检验氯离子.
解答:解:(1)①过滤装置是分离难溶性物质和溶液的分离方法,用到的玻璃仪器为:烧杯、玻璃棒、漏斗,故答案为:玻璃棒;漏斗;
②过量的氯化钡会将全部的硫酸根离子沉淀完毕,只要是硫酸根剩余,则氯化钡会与其反应出现白色沉淀,所以判断BaCl2已过量的方法是:取第②步后的上层清液(或取少量上层清液于试管中),再滴入适量BaCl2溶液,若溶液未变浑浊,则表明BaCl2已过量,
故答案为:取第②步后的上层清液(或取少量上层清液于试管中),再滴入适量BaCl2溶液,若溶液未变浑浊,则表明BaCl2已过量;
③除杂试剂为了根号除去杂质离子,一般是过量的,碳酸钠可以将钙离子以及过量的钡离子沉淀下来,BaCl2、NaOH、Na2CO3加入的顺序必须满足最后加入碳酸钠,过滤后再加盐酸制不再有气体生成即可,故答案为:在氢氧化钠和氯化钡试剂加入后再加入碳酸钠;
④若先用盐酸调pH再过滤,氢氧化镁沉淀、碳酸钙沉淀均会和盐酸反应,将对实验结果产生影响,
故答案为:在此酸度条件下,会有部分沉淀溶解,从而影响制得精盐的纯度;
(2)在检验氯离子时,是加入硝酸银出现白色沉淀,证明氯离子的存在;但是硫酸银是微溶于水的,量多了也就变成沉淀了,所以要先检验硫酸根离子,再检验氯离子;先检验硫酸根离子的存在,加入过量的试剂是硝酸钡;过滤沉淀后,加入硝酸酸化的硝酸银溶液检验氯离子的存在,
故答案为:SO42-;Ba(NO3)2;硝酸酸化的硝酸银溶液.
②过量的氯化钡会将全部的硫酸根离子沉淀完毕,只要是硫酸根剩余,则氯化钡会与其反应出现白色沉淀,所以判断BaCl2已过量的方法是:取第②步后的上层清液(或取少量上层清液于试管中),再滴入适量BaCl2溶液,若溶液未变浑浊,则表明BaCl2已过量,
故答案为:取第②步后的上层清液(或取少量上层清液于试管中),再滴入适量BaCl2溶液,若溶液未变浑浊,则表明BaCl2已过量;
③除杂试剂为了根号除去杂质离子,一般是过量的,碳酸钠可以将钙离子以及过量的钡离子沉淀下来,BaCl2、NaOH、Na2CO3加入的顺序必须满足最后加入碳酸钠,过滤后再加盐酸制不再有气体生成即可,故答案为:在氢氧化钠和氯化钡试剂加入后再加入碳酸钠;
④若先用盐酸调pH再过滤,氢氧化镁沉淀、碳酸钙沉淀均会和盐酸反应,将对实验结果产生影响,
故答案为:在此酸度条件下,会有部分沉淀溶解,从而影响制得精盐的纯度;
(2)在检验氯离子时,是加入硝酸银出现白色沉淀,证明氯离子的存在;但是硫酸银是微溶于水的,量多了也就变成沉淀了,所以要先检验硫酸根离子,再检验氯离子;先检验硫酸根离子的存在,加入过量的试剂是硝酸钡;过滤沉淀后,加入硝酸酸化的硝酸银溶液检验氯离子的存在,
故答案为:SO42-;Ba(NO3)2;硝酸酸化的硝酸银溶液.
点评:本题是一道物质的分离和提纯的方法和基本操作的综合应用题,要求学生具有分析和解决问题的能力,难度较大.

练习册系列答案
相关题目
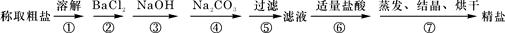
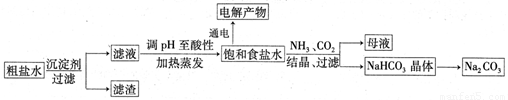
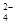 ,得到纯净的NaCl晶体,需加入以下试剂:A.过量的NaOH溶液;B.过量的Na2CO3溶液;C.适量的盐酸;D.过量的BaCl2溶液。
,得到纯净的NaCl晶体,需加入以下试剂:A.过量的NaOH溶液;B.过量的Na2CO3溶液;C.适量的盐酸;D.过量的BaCl2溶液。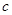 (OH-)的比值是_________。
(OH-)的比值是_________。