题目内容
【题目】(1)写出表示含有 8 个质子、10 个中子的原子的符号__________。
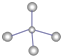
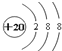
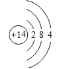
(2)画出 Si 原子的原子结构示意图 ________________________。
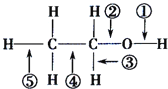
(3)写出 H2O 的电子式 ________
(4)所含元素为 18 种的周期是第________、________周期。
【答案】![]()
![]() 四 五
四 五
【解析】
(1)在表示原子组成时元素符号的左下角表示质子数,左上角表示质量数;
(2)Si的原子序数为14,结合核外电子排布规律分析;
(3)H2O 为共价化合物,分子内共有两个氢氧共用电子对;
(4)根据元素周期表的结构回答。
(1)因质子数和中子数之和是质量数,所以O的质量数为8+10=18,,该原子的原子符号位![]() ,
,
故答案为:![]() ;
;
(2)Si的原子序数为14,在元素周期表第三周期IVA族,其原子结构示意图为: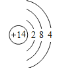 ,
,
故答案为: ;
;
(3)H2O 为共价化合物,其电子式为:![]() ,
,
故答案为:![]() ;
;
(4)在元素周期表中,共有7个周期,第七周期是不完全周期,前六周期中每个周期的元素种类数为:2、8、8、18、18和32,所以所含元素为 18 种的周期是第四和第五周期,
故答案为:四;五。

练习册系列答案
相关题目
【题目】分类法是一种行之有效、简单易行的科学方法。某同学用下表所示形式对所学知识进行分类,其中甲与乙、丙、丁是包含关系。下列各组中,有错误的组合是
选项 | 甲 | 乙、丙、丁 |
A | 常见干燥剂 | 浓硫酸、五氧化二磷、碱石灰 |
B | 常见合金 | 不锈钢、焊锡、生铁 |
C | 常见营养物质 | 蛋白质、维生素、无机盐 |
D | 常见碱 | 烧碱、纯碱、熟石灰 |
A.AB.BC.CD.D