题目内容
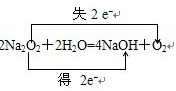
呼吸面具里有Na2O2,可吸收CO2放出O2,若用超氧化钾(KO2)代替过氧化钠,也能吸收CO2生成碳酸盐和O2。
(1)写出KO2与CO2反应的化学方程式。
(2)1 kg Na2O2和1 kg KO2与CO2反应生成O2的质量分别为________。
(3)你认为选用________作为氧化剂更为合适,理由是________。
4KO2+2CO2====2K2CO3+3O2 205 g 338 g KO2 等质量时,KO2产生O2多
(1)由题给信息分析KO2和CO2反应的生成物为K2CO3和O2,并配平该化学方程式。
(2)由2Na2O2—O2 4KO2—3O2
156 32 284 96
1 kg x 1 kg y
解得x="0.205" kg y="0.338" kg。
(3)利用(2)中搭设的台阶,可知等质量时KO2产生O2质量更多,故选KO2更合适。
(1)由题给信息分析KO2和CO2反应的生成物为K2CO3和O2,并配平该化学方程式。
(2)由2Na2O2—O2 4KO2—3O2
156 32 284 96
1 kg x 1 kg y
解得x="0.205" kg y="0.338" kg。
(3)利用(2)中搭设的台阶,可知等质量时KO2产生O2质量更多,故选KO2更合适。

练习册系列答案
相关题目
(12分)某化学兴趣小组在化学实验室发现一瓶没有标签的淡黄色粉末,同学们对探究该粉末产生浓厚兴趣,并在老师的指导下进行探究活动。
【提出问题】这种淡黄色粉末是什么?有什么性质和用途?
【查阅资料】①硫是淡黄色粉末,不溶于水;②过氧化钠(Na2O2)是淡黄色粉末,在常温下能与水反应生成碱和一种气体;在呼吸面具中和潜水艇里常用作供氧剂。
【猜想与探究】猜想:淡黄色粉末可能是:a.硫;b.过氧化钠;c.硫和过氧化钠的混合物。
探究:过氧化钠与水反应的生成物的成分。
【实验与结论】
| | 实验操作 | 实验现象 | 实验结论 |
| 猜想 | 在一支洁净的试管中加入适量的上述淡黄色粉末,再加入足量的蒸馏水 | _____________________ | 猜想a、c不成立,猜想b成立。 |
| 探究 | ①用带火星的木条伸入过氧化钠与水反应的试管中 | 木条复燃 | 生成物有___________ |
| ②往①试管内的溶液中滴加___________ ______________ | _____________________ | 生成物有氢氧化钠 |
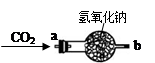
于是设计上图所示的装置继续实验探究。
| 实验操作 | 实验现象 | 实验结论 |
| ①将CO2从a口处通入装置内,再把带火星的木条放在装置b口处 | 木条复燃 | CO2在常温下能与过氧化钠反应,该反应的化学方程式为: ____________________________ |
| ②取出充分反应后的固体生成物于试管中,往试管内滴加稀盐酸,将生成的氢气通入澄清石灰水中 | 有气泡产生 石灰水变浑浊 |