题目内容
12.下列电子式正确的是( )| A. |  | B. |  | ||
| C. | 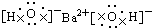 | D. |  |
分析 A、氧化钠为离子化合物,电子式中需要标出阴阳离子所带电荷,Na离子应分开书写,不能合并;
B、硫化氢为共价化合物,分子中存在2个氢硫共用电子对,硫原子最外层一个为8个电子;
C、氢氧化钡为离子化合物,电子式中需要标出阴阳离子所带电荷,且阴离子需要括号;
D、NH3属于共价化合物,分子中存在3对共用电子对,氮原子最外层为8个电子.
解答 解:A、氧化钠为离子化合物,钠离子直接用离子符号表示,阳离子需要标出最外层电子及所带的电荷,此为2个钠离子,Na离子应分开书写,不能合并,故氧化钠的电子式为: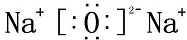 ,故A错误;
,故A错误;
B、H2S为共价化合物,硫原子中最外层有8个电子达到稳定结构,分子中存在两个H-S键,电子式为: ,故B错误;
,故B错误;
C、氢氧化钡为离子化合物,电子式中需要标出阴阳离子所带电荷,且阴离子需要括号,电子式为: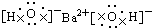 ,故C正确;
,故C正确;
D、NH3属于共价化合物,不存在离子键,分子中存在3对共用电子对,氮原子最外层为8个电子,氨气的电子式为 ,故D错误,故选C.
,故D错误,故选C.
点评 本题考查了电子式的判断,该题是高考中的常见题型与重要的考点,该题基础性强,难易适中,主要是考查学生对常见化学用语的熟悉掌握程度,注意掌握电子式的概念及正确的表示方法.

练习册系列答案
相关题目
2.下列说法中正确的是( )
| A. | PCl3分子是三角锥形,这是因为磷原子是sp2杂化的结果 | |
| B. | 乙烯分子中的碳氢键是氢原子的1s轨道和碳原子的一个个sp3杂化轨道形成的 | |
| C. | 中心原子采取sp3杂化的分子,其几何构型可能是四面体形或三角锥形或V形 | |
| D. | AB3型的分子空间构型必为平面三角形 |
3.下列说法正确的是( )
| A. | 石油裂解得到的汽油是纯净物 | |
| B. | 石油产品都可用于聚合反应 | |
| C. | 天然气是一种清洁的化石燃料 | |
| D. | 水煤气是通过煤的液化得到的气体燃料 |
20.下列关于元素第一电离能的说法不正确的是( )
| A. | 钾元素的第一电离能小于钠元素的第一电离能,故钾的活泼性强于钠 | |
| B. | 因同周期元素的原子半径从左到右逐渐减小,故第一电离能必依次增大 | |
| C. | 最外层电子排布为ns2np6(若只有K层时为1s2)的原子,第一电离能较大 | |
| D. | 对于同一元素而言,原子的逐级电离能越来越大 |
17.将1.92g铜粉与一定浓度的硝酸反应,随着反应的进行,气体颜色逐渐变浅,当铜粉完全作用时收集到气体0.05mol.则所消耗的硝酸的物质的量是( )
| A. | 0.12 mol | B. | 0.11 mol | C. | 0.09 mol | D. | 0.08 mol |
4.下列递变规律不正确的是( )
| A. | Na、Mg、Al还原性依次减弱 | B. | I2、Br2、Cl2氧化性依次增强 | ||
| C. | F、Cl、Br、I原子半径依次增大 | D. | N、O、F最高正价依次升高 |
1.已知氧化铜在高温下可分解为氧化亚铜,取3.76g硝酸铜强热一段时间后得到1.52g固体和NO2、O2的混合气体.将该混合气体用水充分吸收,对残留固体及用水吸收后剩余气体的成分的判断正确的是( )
| 选项 | A | B | C | D |
| 剩余固体 | Cu(NO3)2、CuO | Cu2O、CuO | Cu2O、CuO | Cu(NO3)2、Cu2O |
| 剩余气体 | 无气体剩余 | 氧气2.5×10-3mol | NO 2.5×10-3mol | 氧气2.5×10-3mol |
| A. | A | B. | B | C. | C | D. | D |