题目内容
在28.4 gCaCO3和MgCO3组成的混合物中加入足量稀盐酸,生成气体全部被250 mL 2 mol/L NaOH溶液吸收,将此溶液在减压、低温条件下蒸干得到29.6 g不含结晶水的固体物质.求原混合物中各种物质各多少克?
答案:
解析:
提示:
解析:
|
原混合物中CaCO3为20 g、MgCO3为8.4 g |
提示:
|
NaOH物质的量为0.5 mol,所以固体物质也应含有0.5 mol的钠离子,下面进行讨论: (1)NaOH过量,0.5 mol NaOH质量为20 g,而0.25 mol Na2CO3质量为26.5 g,NaOH和Na2CO3混合不可能得到29.6 g固体物质.这个假设不成立. (2)CO2过量,固体物质可能为Na2CO3和NaHCO3,0.25 mol Na2CO3质量为26.5 g,0.5 gNaHCO3质量为42 g,这个假设成立. 通过上述讨论可知29.6 g固体物质是Na2CO3和NaHCO3的混合物,有关反应为: CO2+2NaOH 利用方程式计算CO2的物质的量为0.3 mol,生成二氧化碳的有关反应为: CaCO3+2HCl MgCO3+2HCl |

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案
相关题目


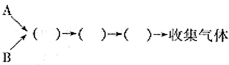

 哥本哈根会议虽未能就减排问题达成有约束力的协议,但各国对于CO2对气候的影响达成了共识,都在积极研究方法循环利用CO2.CO2(g)与H2(g)反应可生成CH3OH(g)和H2O(g).某实验小组为研究该反应进行了如下实验.在某温度下,向容积为10L的恒温恒容容器中充入a mol CO2和a mol H2,测得不同时刻的c(H2)如右表.
哥本哈根会议虽未能就减排问题达成有约束力的协议,但各国对于CO2对气候的影响达成了共识,都在积极研究方法循环利用CO2.CO2(g)与H2(g)反应可生成CH3OH(g)和H2O(g).某实验小组为研究该反应进行了如下实验.在某温度下,向容积为10L的恒温恒容容器中充入a mol CO2和a mol H2,测得不同时刻的c(H2)如右表. CH3OH+H2O
CH3OH+H2O
 收集气体(填写装置编号)
收集气体(填写装置编号)