题目内容
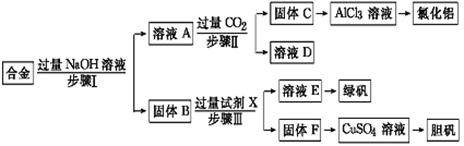
为探索工业废料的再利用,某化学兴趣小组设计了如下实验流程,用含有铝、铁和铜的合金废料制取氯化铝、绿矾晶体(FeSO4·7H2O)和胆矾晶体。
请回答:
(1)写出步骤Ⅰ反应的离子方程式: 。
(2)试剂X是 。步骤Ⅰ、Ⅱ、Ⅲ中均需进行的实验操作是 。
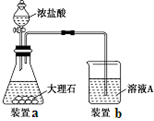
(3)进行步骤Ⅱ时,该小组用如图所示装置及试剂制取CO2并将制得的气体通入溶液A中。一段时间后,观察到烧杯中产生的白色沉淀会逐渐减少。为了避免固体C减少,可采取的改进措施是 。
(4)用固体F制备CuSO4溶液,可设计以下三种途径:

写出途径①中反应的离子方程式 ,请选出你认为的最佳途径并说明选择的理由 。

请回答:
(1)写出步骤Ⅰ反应的离子方程式: 。
(2)试剂X是 。步骤Ⅰ、Ⅱ、Ⅲ中均需进行的实验操作是 。
(3)进行步骤Ⅱ时,该小组用如图所示装置及试剂制取CO2并将制得的气体通入溶液A中。一段时间后,观察到烧杯中产生的白色沉淀会逐渐减少。为了避免固体C减少,可采取的改进措施是 。

(4)用固体F制备CuSO4溶液,可设计以下三种途径:

写出途径①中反应的离子方程式 ,请选出你认为的最佳途径并说明选择的理由 。
(1)2Al+2OH—+2H2O=2AlO2-+3H2↑(2分)
(2)稀硫酸或H2SO4(2分) 过滤(2分)
(3)在装置Ⅰ、Ⅱ之间增加一个盛有饱和NaHCO3溶液的洗气瓶(合理答案即给分)(2分)
(4)3Cu+2NO3-+8H+=3Cu2++2NO↑+4H2O(2分) 途径②最佳,理由是原料利用率高,环境污染小(2分,结论1分,理由1分)
试题分析:(1)铝、铁、铜中铝与氢氧化钠反应,产生偏氯酸钠和氢气;(2)步骤Ⅲ分离铜、铁,且生成绿矾(硫酸亚铁),故x为稀硫酸;固液分离用过滤;(3)由于浓盐酸易挥发,制备的二氧化碳中含有HCl气体,导致生成的氢氧化铝溶解;为了避免固体减少,可采取的除去HCl气体的方法,在装置Ⅰ、Ⅱ之间增加一个盛有饱和NaHCO3溶液的洗气瓶;(4)途径①③产生NO、SO2污染性气体,途径②最佳,理由是原料利用率高,环境污染小。

练习册系列答案
 导学教程高中新课标系列答案
导学教程高中新课标系列答案
相关题目




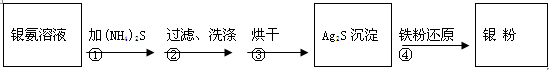
 2 Ag+ FeCl2+H2S↑。
2 Ag+ FeCl2+H2S↑。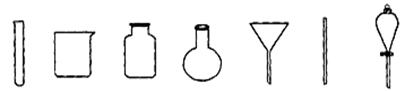
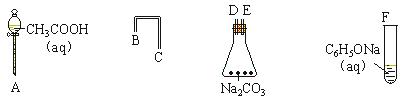
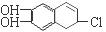 分别与浓溴水和NaOH溶液完全反应,消耗Br2和NaOH的物质的量分别是 mol和 mol。
分别与浓溴水和NaOH溶液完全反应,消耗Br2和NaOH的物质的量分别是 mol和 mol。