题目内容
下列各组离子中,在碱性溶液中能大量共存,且溶液为无色透明的是
| A.K+ MnO4- Cl- SO42- | B.Na+ AlO2- Cl-SO42- |
| C.SO42-Na+HCO3-Ba2+ | D.Na+ NO3- NH4+ SO42- |
B
解析试题分析:离子间如果发生化学反应,则不能大量共存,反之是可以的。A中MnO4-在溶液中显紫色,C中SO42-与Ba2+不能大量共存,且在碱性条件下,HCO3-不能大量共存,D中在碱性条件下,NH4+不能大量共存,所以答案选B。
考点:考查离子共存的正误判断
点评:该题是高考中的高频题,属于中等难度的试题,侧重对学生基础知识的训练和检验。有利于培养学生的逻辑推理能力,提高学生灵活运用基础知识解决实际问题的能力。该题需要明确离子不能大量共存的一般情况,即(1)能发生复分解反应的离子之间;(2)能生成难溶物的离子之间;(3)能发生氧化还原反应的离子之间;(4)能发生络合反应的离子之间(如 Fe3+和 SCN-);解决离子共存问题时还应该注意题目所隐含的条件,题目所隐含的条件一般有:(1)溶液的酸碱性,据此来判断溶液中是否有大量的 H+或OH-;(2)溶液的颜色,如无色时可排除 Cu2+、 Fe2+、Fe3+、MnO4-等有色离子的存在;(3)溶液的具体反应条件,如“氧化还原反应”、“加入铝粉产生氢气”;(4)是“可能”共存,还是“一定”共存等。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
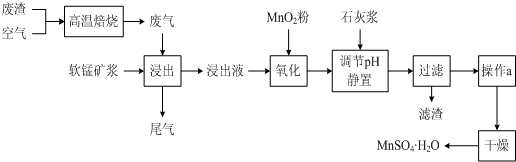
为了回收利用SO2,研究人员研制了利用低品位软锰矿浆(主要成分是MnO2)吸收高温焙烧含硫废渣产生的SO2废气,制备硫酸锰晶体的生产流程,其流程示意图如下:

已知,浸出液的pH<2,其中的金属离子主要是Mn2+,还含有少量的Fe2+、Al3+等其他金属离子.有关金属离子形成氢氧化物沉淀时的pH见下表:
请回答下列问题:
(1)写出浸出过程中主要反应的化学方程式:______.
(2)写出氧化过程中主要反应的离子方程式:______.
(3)在氧化后的液体中加入石灰浆,用于调节pH,pH应调节至______.
(4)滤渣的主要成分有______.
(5)下列各组试剂中,能准确测定尾气中SO2含量的是______.(填编号)
a.NaOH溶液、酚酞试液 b.稀H2SO4酸化的KMnO4溶液 c.碘水、淀粉溶液 d.氨水、酚酞试液
(6)已知废气中SO2浓度为6.4g/m3,软锰矿浆对SO2的吸收率可达90%,则处理1000m3废气,可得到硫酸锰晶体质量为______kg.

已知,浸出液的pH<2,其中的金属离子主要是Mn2+,还含有少量的Fe2+、Al3+等其他金属离子.有关金属离子形成氢氧化物沉淀时的pH见下表:
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH | 加碱溶解的pH |
| Fe2+ | 7.6 | 9.7 | |
| Fe3+ | 2.7 | 3.7 | |
| Al3+ | 3.8 | 4.7 | >8.5 |
| Mn2+ | 8.3 | 9.8 |
(1)写出浸出过程中主要反应的化学方程式:______.
(2)写出氧化过程中主要反应的离子方程式:______.
(3)在氧化后的液体中加入石灰浆,用于调节pH,pH应调节至______.
(4)滤渣的主要成分有______.
(5)下列各组试剂中,能准确测定尾气中SO2含量的是______.(填编号)
a.NaOH溶液、酚酞试液 b.稀H2SO4酸化的KMnO4溶液 c.碘水、淀粉溶液 d.氨水、酚酞试液
(6)已知废气中SO2浓度为6.4g/m3,软锰矿浆对SO2的吸收率可达90%,则处理1000m3废气,可得到硫酸锰晶体质量为______kg.