题目内容
11.下列反应前后物质的总能量变化可用如图表示的是( )
| A. | H-F═H+F | B. | Mg+2H+=Mg2++H2↑ | ||
| C. | 2Na+2H2O=2Na++2OH-+H2↑ | D. | HNO3+NaOH=NaNO3+H2O |
分析 生成物总能量高于反应物总能量,应为吸热反应.
常见的放热反应有:所有的物质燃烧;所有金属与酸或与水;所有中和反应;绝大多数化合反应;铝热反应;
常见的吸热反应有:绝大数分解反应;个别的化合反应(如C和CO2);工业制水煤气;碳、一氧化碳、氢气还原金属氧化物;某些复分解(如铵盐和强碱).
解答 解:A.断键吸收能量,是吸热过程,故A正确;
B.镁和酸反应属于放热反应,故B错误;
C.金属钠与水反应属于放热反应,故C错误;
D.HNO3+NaOH=NaNO3+H2O是中和反应,属于放热反应,故D错误.
故选A.
点评 本题考查放热反应,难度不大,抓住中学化学中常见的吸热或放热的反应是解题的关键,对于特殊过程中的热量变化的要熟练记忆来解答此类习题.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
2.下列说法正确的是( )
| A. | 淀粉、油脂和蛋白质都是高分子化合物 | |
| B. | 乙酸乙酯和植物油水解均可生成乙醇 | |
| C. | “地沟油”的主要成分是油脂,其类别与煤油不同 | |
| D. | 煤中含有煤焦油及多种化工原料,可通过煤的干馏获得 |
19.关于下列各装置图的叙述中,不正确的是( )
| A. | 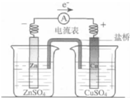 图中总反应为Zn+CuSO4═Cu+ZnSO4 | |
| B. | 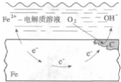 图中正极反应为2H2O+O 2+4e-═4OH- | |
| C. | 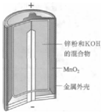 图中负极反应为Zn+2OH--2e-═Zn(OH)2 | |
| D. |  图中向Fe电极区滴入2滴铁氰化钾溶液产生蓝色沉淀 |
6.根据下列实验及现象,能量关系正确的是( )
| 实验及现象 | 能量关系 | |
| A | 将“NO2球”置于热水中,红棕色加深 | N2O4(g)?2NO2(g)△H<0 |
| B | NaOH与HCl溶液混合,溶液温度升高 |  |
| C | 钠投入水中,熔化成小球 |  |
| D | 微热含酚酞的Na2CO3溶液,红色加深 | CO32-(aq)+H2O(l)?HCO3-(aq)+OH-(aq)△H<0 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
16.如图,下列装置属于原电池的是( )
| A. | 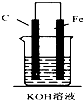 | B. | 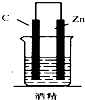 | C. | 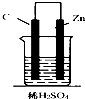 | D. |  |
3.已知金刚石的燃烧热为395kJ/mol,下表是部分化学键的键能数据.下列选项中正确的是( )
| 化学键 | C-C | O=O | C=O |
| 键能(kJ/mol) | 348 | 498 | x |
| A. | x=794.5 | |
| B. | x=1142.5 | |
| C. | 1mol金刚石的能量一定比1mol CO2能量高 | |
| D. | 金刚石燃烧的热化学方程式为 2C(s)+O2(g)=2CO(g)△H=-790 kJ/mol |
20.下列说法中正确的是( )
| A. | CH3COOH和CH3COONH4都是弱电解质 | |
| B. | Na2O2既含离子键又含共价键 | |
| C. | HBr、HCl、HF的酸性依次增强 | |
| D. | 二氧化硅有导电性,可用于制备光导纤维 |
1.化学服务于生产、生活,下列有关说法正确的是( )
| A. | 改燃煤为燃气,可以减少二氧化硫等有害气体的排放,是治理“雾霾”的措施之一 | |
| B. | 石英雕刻工艺是利用了浓硫酸的强腐蚀性 | |
| C. | 光分解水制氢气、植物秸秆制沼气、高粱制乙醇涉及到生物质能的利用 | |
| D. | 硬铝、碳素钢都是合金材料,合成纤维、光导纤维都是有机高分子化合物 |