题目内容
16.建筑用红砖中含有Fe2O3,若要检验红砖中+3价铁元素的存在,应该选用的试剂及其顺序为( )(供选择的试剂:①KSCN溶液②H2O2溶液③盐酸④酸性KMnO4溶液)
| A. | ①④ | B. | ③① | C. | ③②① | D. | ③①④ |
分析 红砖中含有Fe2O3,若要检验红砖中+3价铁元素的存在,溶于盐酸或稀硫酸后,加KSCN溶液,出现血红色即可,以此来解答.
解答 解:红砖中含有Fe2O3,若要检验红砖中+3价铁元素的存在,溶于盐酸或稀硫酸后,加KSCN溶液,出现血红色即可,则选用的试剂及其顺序为③①,
故选B.
点评 本题考查物质的性质及离子检验,为高频考点,把握铁离子的检验方法为解答的关键,侧重分析与实验能力的考查,注意离子检验的特征试剂,题目难度不大.

练习册系列答案
相关题目
8.KMnO4具有强氧化性,在实验室和工业上常用作氧化剂.某化学兴趣小组采用标准的酸性KMnO4溶液测定可能发生变质的还原性物质Na2SO3固体中Na2SO3的含量.
(1)简述检验Na2SO3已经变质的操作和现象:取少量样品于试管中,加水溶解,先加入过量盐酸,再加入氯化钡溶液,如果有白色沉淀生成,表明Na2SO3已经变质.
(2)另取10.0g试样配成250mL溶液,配制溶液时,可能用到的玻璃仪器有量筒、烧杯、玻璃棒、250 mL容量瓶、胶头滴管.取出25.00mL所配制的Na2SO3溶液于锥形瓶中,用标准酸性KMnO4溶液滴定,采用的指示剂是无(如果不需要,可写“无”).判断滴定实验达到终点的方法是当最后一滴酸性KMnO4溶液滴入锥形瓶后,瓶内溶液变成浅粉红色且半分钟内不褪色.反应的离子方程式为SO32-+MnO4-+H+→SO42-+Mn2++H2O(未配平).重复操作四次,消耗0.10mol•L-1 KMnO4溶液的体积如下:
求样品中Na2SO3的质量分数63%.
(3)操作时,若未用0.10mol•L-1的酸性KMnO4溶液润洗滴定管,会导致测定结果偏高(填“偏高”、“偏低”或“没有影响”).
(1)简述检验Na2SO3已经变质的操作和现象:取少量样品于试管中,加水溶解,先加入过量盐酸,再加入氯化钡溶液,如果有白色沉淀生成,表明Na2SO3已经变质.
(2)另取10.0g试样配成250mL溶液,配制溶液时,可能用到的玻璃仪器有量筒、烧杯、玻璃棒、250 mL容量瓶、胶头滴管.取出25.00mL所配制的Na2SO3溶液于锥形瓶中,用标准酸性KMnO4溶液滴定,采用的指示剂是无(如果不需要,可写“无”).判断滴定实验达到终点的方法是当最后一滴酸性KMnO4溶液滴入锥形瓶后,瓶内溶液变成浅粉红色且半分钟内不褪色.反应的离子方程式为SO32-+MnO4-+H+→SO42-+Mn2++H2O(未配平).重复操作四次,消耗0.10mol•L-1 KMnO4溶液的体积如下:
| 编号溶液 | 1 | 2 | 3 | 4 |
| KMnO4(mL) | 20.01 | 19.00 | 19.99 | 20.00 |
| Na2SO3(mL) | 25.00 | 25.00 | 25.00 | 25.00 |
(3)操作时,若未用0.10mol•L-1的酸性KMnO4溶液润洗滴定管,会导致测定结果偏高(填“偏高”、“偏低”或“没有影响”).
4.下列判断错误的是( )
| A. | 稳定性:NH3>PH3>AsH3 | B. | 离子半径:Li+>O2->F- | ||
| C. | 酸性:H3PO4<H2SO4<HClO4 | D. | 碱性:LiOH<NaOH<KOH |
11.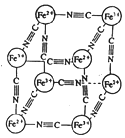 分析化学中常用 X 射线研究晶体结构,有一种蓝色晶体[可表示为:MxFey(CN)z],研究表明它的结构特性是:Fe2+和 Fe3+分别占据立方体的顶点,自身互不相邻,而 CN-位 于立方体的棱上.晶体的晶胞结构如图所示,下列说法不正确的是( )
分析化学中常用 X 射线研究晶体结构,有一种蓝色晶体[可表示为:MxFey(CN)z],研究表明它的结构特性是:Fe2+和 Fe3+分别占据立方体的顶点,自身互不相邻,而 CN-位 于立方体的棱上.晶体的晶胞结构如图所示,下列说法不正确的是( )
 分析化学中常用 X 射线研究晶体结构,有一种蓝色晶体[可表示为:MxFey(CN)z],研究表明它的结构特性是:Fe2+和 Fe3+分别占据立方体的顶点,自身互不相邻,而 CN-位 于立方体的棱上.晶体的晶胞结构如图所示,下列说法不正确的是( )
分析化学中常用 X 射线研究晶体结构,有一种蓝色晶体[可表示为:MxFey(CN)z],研究表明它的结构特性是:Fe2+和 Fe3+分别占据立方体的顶点,自身互不相邻,而 CN-位 于立方体的棱上.晶体的晶胞结构如图所示,下列说法不正确的是( )| A. | 该晶体中含有共价键,是离子晶体 | |
| B. | M 离子位于晶胞面心,呈+2 价 | |
| C. | M 离子位于晶胞体心,呈+1 价,且 M+空缺率为 50%(体心中没有 M+占总体心的百分比) | |
| D. | 晶体的化学式可表示为 MFe2(CN)6,且 M 为+1 价 |
1.已知aAn+、bB(n+1)+、cCn-、dD(n+1)-均具有相同的电子层结构,下列关于A、B、C、D四种元素的叙述不正确的是( )
| A. | 原子半径:A>B>D>C | B. | 原子序数:b>a>c>d | ||
| C. | 离子半径:D(n+1)->Cn->An+>B(n+1)+ | D. | 金属性:B>A,非金属性:D>C |
8.下列各组物质中互为同位素的是( )
| A. | ${\;}_{20}^{40}$Ca 和${\;}_{18}^{40}$Ar | B. | D和T | ||
| C. | H2 O和H2 O2 | D. | O3 和O2 |
5.下列物质中,不能使有色布条褪色的是( )
| A. | 次氯酸钠溶液 | B. | 次氯酸钙溶液 | C. | 氯水 | D. | 氯化钙 |
6.设NA为阿伏加德罗常数的值.下列说法正确的是( )
| A. | 质量a g的C2H4和C3H6的混合物中共用电子对数目为$\frac{3a{N}_{A}}{14}$ | |
| B. | 常温下,0.1 mol•L-1的NaOH溶液中含有OH一的数目为0.1NA | |
| C. | 常温常压下,14g由N2与CO组成的混合气体含有的原子数目为2NA | |
| D. | 7.8g过氧化钠固体中阴、阳离子总数为0.4NA |
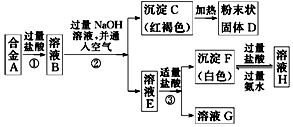 铁和铝是日常生活中用途广泛的金属.
铁和铝是日常生活中用途广泛的金属.