题目内容
1.已知aAn+、bB(n+1)+、cCn-、dD(n+1)-均具有相同的电子层结构,下列关于A、B、C、D四种元素的叙述不正确的是( )| A. | 原子半径:A>B>D>C | B. | 原子序数:b>a>c>d | ||
| C. | 离子半径:D(n+1)->Cn->An+>B(n+1)+ | D. | 金属性:B>A,非金属性:D>C |
分析 已知aAn+、bB(n+1)+、cCn-、dD(n+1)-具有相同的电子层结构,则有:a-n=b-(n+1)=c+n=d+(n+1),则有A、B在周期表中C、D的下一周期,并且原子序数:b>a>c>d,结合元素周期律递变规律解答该题.
解答 解:已知aAn+、bB(n+1)+、cCn-、dD(n+1)-具有相同的电子层结构,则有:a-n=b-(n+1)=c+n=d+(n+1),则有A、B在周期表中C、D的下一周期,并且原子序数:b>a>c>d,则
A.电子层越多,原子半径越大,同周期从左向右原子半径减小,则原子半径为A>B>D>C,故A正确;
B.由以上分析可知原子序数:b>a>c>d,故B正确;
C.aAn+、bB(n+1)+、cCn-、dD(n+1)-具有相同的电子层结构,核电荷数越大离子半径越小,核电荷数b>a>c>d,故离子半径D(n+1)->Cn->An+>B(n+1)+,故C正确;
D.A、B在周期表中同周期,原子序数:b>a,金属性:A>B,C、D在同一周期,且原子序数C>D,非金属性:C>D,故D错误.
故选D.
点评 本题考查原子结构与元素周期律,为高频考点,把握具有相同电子排布的离子的相对位置、元素周期律为解答的关键,侧重分析与应用能力的考查,注意规律性知识的应用,题目难度不大.

练习册系列答案
相关题目
13. 向含Na2CO3、NaAlO2的混合溶液中逐滴加入150mL 1mol•L-1的HC1溶液,测得溶液中某几种离子的物质的量变化如图所示,则下列说法不正确的是( )
向含Na2CO3、NaAlO2的混合溶液中逐滴加入150mL 1mol•L-1的HC1溶液,测得溶液中某几种离子的物质的量变化如图所示,则下列说法不正确的是( )
 向含Na2CO3、NaAlO2的混合溶液中逐滴加入150mL 1mol•L-1的HC1溶液,测得溶液中某几种离子的物质的量变化如图所示,则下列说法不正确的是( )
向含Na2CO3、NaAlO2的混合溶液中逐滴加入150mL 1mol•L-1的HC1溶液,测得溶液中某几种离子的物质的量变化如图所示,则下列说法不正确的是( )| A. | b和c曲线表示的离子反应均为CO32-+H+═HCO3- | |
| B. | 结合H+的能力:A1O2->CO32->HCO3->Al(OH)3 | |
| C. | M点时Al(OH)3的质量等于3.9 g | |
| D. | 原混合溶液中,CO32-与A1O2-的物质的量之比为2:1 |
12.下列说法正确的是( )
| A. | 向苯酚钠溶液中通入CO2可制得苯酚,并得到碳酸钠 | |
| B. | 将铁屑、溴水、苯混合可制得溴苯 | |
| C. | 实验时不小心沾到手上的苯酚可用氢氧化钠溶液洗掉 | |
| D. | 用醋酸溶液洗涤沾附在暖水瓶内壁上水垢的过程中发生了复分解反应 |
9.关于化学式[TiCl( H2O)5]Cl2•H2O 的配合物的下列说法中正确的是( )
| A. | 配位体是 Cl-和 H2 O,配位数是8 | |
| B. | 中心离子是 Ti4+,配离子是[TiCl(H2 O)5]2+ | |
| C. | 内界和外界中的 Cl-的数目比是 1:2 | |
| D. | 在 1mol 该配合物中加入足量 AgNO3 溶液,可以得到 3molAgCl 沉淀 |
16.建筑用红砖中含有Fe2O3,若要检验红砖中+3价铁元素的存在,应该选用的试剂及其顺序为( )
(供选择的试剂:①KSCN溶液②H2O2溶液③盐酸④酸性KMnO4溶液)
(供选择的试剂:①KSCN溶液②H2O2溶液③盐酸④酸性KMnO4溶液)
| A. | ①④ | B. | ③① | C. | ③②① | D. | ③①④ |
6. 氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如图.下列有关氢氧燃料电池的说法不正确的是( )
氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如图.下列有关氢氧燃料电池的说法不正确的是( )
 氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如图.下列有关氢氧燃料电池的说法不正确的是( )
氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如图.下列有关氢氧燃料电池的说法不正确的是( )| A. | 该装置将化学能转化为电能 | |
| B. | 为了增加灯泡亮度,可以将电极碳棒变得多粗糙多孔 | |
| C. | 电子迁移方向:电极a→灯泡→电极b→电解质溶液→电极a | |
| D. | 该电池的总反应:2H2+O2═2H2O |
13.己烷雌酚的一种合成路线如下:

下列叙述正确的是( )

下列叙述正确的是( )
| A. | 在NaOH水溶液中加热,化合物X可发生消去反应 | |
| B. | 在一定条件下,化合物Y可与HCHO发生缩聚反应 | |
| C. | 用FeCl3溶液不可鉴别化合物X和Y | |
| D. | 化合物Y中不含有手性碳原子 |
10.在下列条件下,一定能大量共存的微粒组是( )
| A. | 常温下,水电离的c(H+)=1×10-14mol/L的溶液中:K+、Na+、AlO2-、SiO32- | |
| B. | 使甲基橙变红的溶液中:Na+、Fe3+、NO3-、SO32- | |
| C. | 常温下,在$\frac{c({H}^{+})}{c(O{H}^{-})}$=10-12的溶液中:K+、Ba2+、NO3-、I- | |
| D. | 中性的溶液中:CO32-、Na+、SO42-、AlO2- |
11.用下列实验装置进行相应的实验,能达到实验目的是( )
| A. |  用于实验室制氨气并收集干燥的氨气 | |
| B. |  用于除去CO2中含有的少量HC1 | |
| C. |  用于提取I2的CCl4溶液中的I2 | |
| D. | 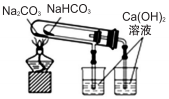 装置用于验证NaHCO3和Na2CO3的热稳定性 |