题目内容
14.0 g铜银合金与足量某浓度的硝酸反应,将放出的气体与1.12 L(标准状况)氧气混合,通入水中恰好完全吸收,则合金中铜的质量为( )
A.9.6 g B.6.4 g C.3.2 g D.1.6 g
C
解析:
由题意知,Cu、Ag与HNO3反应所得还原产物与O2作用溶于水后又变为HNO3,因此可以认为Cu、Ag所失电子最终被O2而非HNO3所得。
设Cu、Ag物质的量分别为x、y,则:
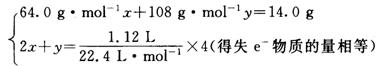
解得:x=0.050 mol, m(Cu)=64 g·mol-1×0.050 mol=3.2 g

练习册系列答案
 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案
相关题目
 N2O4(g) 的平衡常数K=13.3,该条件下密闭容器中N2O4和NO2的混合气体达到平衡时c(NO2)="0.0300" mol·L-1。
N2O4(g) 的平衡常数K=13.3,该条件下密闭容器中N2O4和NO2的混合气体达到平衡时c(NO2)="0.0300" mol·L-1。