题目内容
反应4NH3+5O2 4NO+6H2O(g),在5L的密闭容器中进行半分钟后,NO的物质的量增加了0.3mol,则此反应的平均速率υ(x)(表示反应物的消耗速率或生成物的生成速率)为 ( )
4NO+6H2O(g),在5L的密闭容器中进行半分钟后,NO的物质的量增加了0.3mol,则此反应的平均速率υ(x)(表示反应物的消耗速率或生成物的生成速率)为 ( )
| A.υ(O2)="0.001" mol·L-1·s-1 | B.υ(NO)="0.06" mol·L-1·s-1 |
| C.υ(H2O) ="0.003" mol·L-1·s-1 | D.υ(NH3)="0.001" mol·L-1·s-1 |
C
解析试题分析:在5L的密闭容器中进行,半分钟后NO的物质的量增加了0.3mol,代入反应速率计算公式可得v(NO)="0.002" mol·L-1·s-1;由反应速率之比等于化学计量数之比可知,v(NO)=v(NH3)="0.002" mol·L-1·s-1,v(H2O)="0.003" mol·L-1·s-1,v(O2)="0.0025" mol·L-1·s-1,选C。
考点:考查化学反应速率的计算。

 优翼小帮手同步口算系列答案
优翼小帮手同步口算系列答案反应2SO2(g)+O2 2SO3(g)经一段时间后,SO3的浓度增加了0.4mol/L,在这段时间内用O2表示的反应速率为0.04mol/(L·s),则这段时间为( )
2SO3(g)经一段时间后,SO3的浓度增加了0.4mol/L,在这段时间内用O2表示的反应速率为0.04mol/(L·s),则这段时间为( )
| A.0.1s | B.2.5s | C.10s | D.5s |
工业上利用可逆反应N2(g)+3H2(g)  2NH3(g)合成氨,下列叙述正确的是
2NH3(g)合成氨,下列叙述正确的是
| A.合成氨的适宜条件是高温、高压、催化剂,其中催化剂不改变该反应的逆反应速率 |
| B.恒容通入氩气,使反应体系的压强增大,反应速率一定增大 |
| C.该反应是放热反应,降低温度将缩短反应达到平衡的时间 |
D.在t1、t2时刻,NH3 (g)的浓度分别是c1、c2,则时间间隔t1~t2内,NH3 (g)生成的平均速率为v=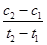 |
N2O5是一种新型硝化剂,在一定温度下可发生以下反应:
2N2O5(g)  4NO2 (g)+ O2(g) ΔH > 0
4NO2 (g)+ O2(g) ΔH > 0
T1温度时,向密闭容器中通入N2O5,部分实验数据见下表:
| 时间/s | 0 | 500 | 100 0 | 150 0 |
| c(N2O5)/ mol·L-1 | 5.00 | 3.52 | 2.50 | 2.50 |
下列说法中不正确的是
A.500 s内N2O5分解速率为2.96╳10-3mol·L-1·s-1
B.T1温度下的平衡常数为K1=125,平衡时N2O5的转化率为50%
C.T1温度下的平衡常数为K1,T2温度下的平衡常数为K2,若T1>T2,则K1<K2
D.达平衡后其他条件不变,将容器的体积压缩到原来的1/2,则c(N2O5)> 5.00 mol·L-1
在一定条件下,已达平衡的可逆反应:2A(g)+B(g)  2C(g),下列说法中正确的是 ( )
2C(g),下列说法中正确的是 ( )
A.平衡时,此反应的平衡常数K与各物质的浓度有如下关系:K=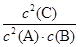 |
| B.改变条件后,该反应的平衡常数K一定不变 |
| C.如果改变压强并加入催化剂,平衡常数会随之变化 |
| D.若平衡时增加A和B的浓度,则平衡常数会减小 |
某可逆反应aA+bB cC+Q在某温度下的平衡常数为K(K≠1),反应热为Q。保持温度不变,将方程式的书写作如下改变,则Q和K数值的相应变化为
cC+Q在某温度下的平衡常数为K(K≠1),反应热为Q。保持温度不变,将方程式的书写作如下改变,则Q和K数值的相应变化为
A.写成2aA+2bB 2cC,Q值、K值均扩大了一倍 2cC,Q值、K值均扩大了一倍 |
B.写成2aA+2bB 2cC,Q值扩大了一倍,K值保持不变 2cC,Q值扩大了一倍,K值保持不变 |
C.写成cC aA+bB,Q值、K值变为原来的相反数 aA+bB,Q值、K值变为原来的相反数 |
D.写成cC aA+bB,Q值变为原来的相反数,K值变为倒数 aA+bB,Q值变为原来的相反数,K值变为倒数 |
将X和Y以1:2的体积比混合后置于密闭容器中,加压到3×107Pa,发生如下反应:X(g)+2Y(g)?2Z(g),达到平衡状态时,测得反应物的总物质的量和生成物的总物质的量相等,有关数据如图,则反应对应的温度是( )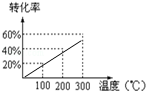
| A.100℃ | B.200℃ | C.300℃ | D.不能确定 |
图为某化学反应速率一时间图。在 时刻升高温度或增大压强,都符合下图所示变化的反应是
时刻升高温度或增大压强,都符合下图所示变化的反应是
A.2SO2(g)+O2(g) 2SO3(g);ΔH<0 2SO3(g);ΔH<0 |
B.4NH3(g)+5O2(g) 4NO(g)+6H2O(g);ΔH<0 4NO(g)+6H2O(g);ΔH<0 |
C.H2(g)+I2(g) 2HI(g); ΔH>0 2HI(g); ΔH>0 |
D.C(s)+H2O(g) CO(g)+H2(g) ;ΔH>0 CO(g)+H2(g) ;ΔH>0 |
对于可逆反应:aA(g)+bB(g) mC(g)+ nD(g);△H<0,下列说法正确的是
mC(g)+ nD(g);△H<0,下列说法正确的是
| A.浓度改变平衡必移动 | B.增大压强平衡必移动 |
| C.升高温度平衡必移动 | D.导入氦气平衡必移动 |