题目内容
下列物质属于强酸的是( )
| A、碳酸 | B、碳酸氢钠 |
| C、硫酸钡 | D、硫酸 |
考点:电解质与非电解质,酸、碱、盐、氧化物的概念及其相互联系
专题:物质的分类专题
分析:强酸是在水溶液中完全电离出的阳离子全是氢离子的化合物,据此即可解答.
解答:
解:A.碳酸电离方程式:H2CO3 H++HCO3-,HCO3-H++CO32-,碳酸为多元弱酸分步电离,故A错误;
B.碳酸氢钠电离方程式:NaHCO3=Na++HCO3-,所以碳酸氢钠属于盐,故B错误;
C.硫酸钡电离方程式:BaSO4=Ba2++SO42-,所以硫酸钡属于盐,故C错误;
D.硫酸电离方程式:H2SO4=2H++SO42-,所以硫酸是强酸,故D正确;
故选:D.
B.碳酸氢钠电离方程式:NaHCO3=Na++HCO3-,所以碳酸氢钠属于盐,故B错误;
C.硫酸钡电离方程式:BaSO4=Ba2++SO42-,所以硫酸钡属于盐,故C错误;
D.硫酸电离方程式:H2SO4=2H++SO42-,所以硫酸是强酸,故D正确;
故选:D.
点评:本题主要考查了强酸概念,抓住强酸完全电离出的阳离子全部为氢离子是解题的关键,题目难度不大.

练习册系列答案
相关题目
下列有关实验操作不正确的是( )
| A、蒸发操作时,应在混合物中有晶体析出时立即停止加热 |
| B、在萃取实验中,萃取剂要求与原溶剂互不相溶,且溶质在萃取剂中的溶解度更大 |
| C、开始蒸馏时,应该先开冷凝水,再加热;蒸馏完毕,应该先撤酒精灯再关冷凝水 |
| D、分液操作时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 |
浓硫酸滴到纸片上,纸片马上变黑,这是因为浓硫酸具有( )
| A、脱水性 | B、吸水性 |
| C、强酸性 | D、强氧化性 |
某种ABS工程树脂,由丙烯腈(CH2=CHCN,符号A)、1,3-丁二烯(CH2=CHCH=CH2,符号B)和苯乙烯(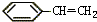 ,符号S)按一定配比共聚而得.经元素分析可知该ABS样品的组成为CaHbNc(a、b、c为正整数),则原料中A和B的物质的量之比用a、b、c表示是( )
,符号S)按一定配比共聚而得.经元素分析可知该ABS样品的组成为CaHbNc(a、b、c为正整数),则原料中A和B的物质的量之比用a、b、c表示是( )
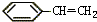 ,符号S)按一定配比共聚而得.经元素分析可知该ABS样品的组成为CaHbNc(a、b、c为正整数),则原料中A和B的物质的量之比用a、b、c表示是( )
,符号S)按一定配比共聚而得.经元素分析可知该ABS样品的组成为CaHbNc(a、b、c为正整数),则原料中A和B的物质的量之比用a、b、c表示是( )A、
| ||
B、
| ||
C、
| ||
| D、无法确定 |
实验室中需2mol/L的CuSO4溶液950ml,配制时应选用的容量瓶的规格和称取的CuSO4?5H2O的质量分别是( )
| A、1000ml,500g |
| B、950ml,475g |
| C、1000ml,490g |
| D、50 ml,304g |
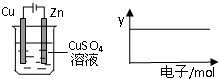 按如图装置实验,若x轴表示流入阴极的电子的物质的量,(假设溶液的体积不变)则不能用y轴表示的是( )
按如图装置实验,若x轴表示流入阴极的电子的物质的量,(假设溶液的体积不变)则不能用y轴表示的是( )| A、c(Cu2+) |
| B、c(SO42-) |
| C、Cu棒的质量 |
| D、溶液的pH |
抗酸药中既能与强酸反应,又能与强碱反应得物质是( )
| A、CaCO3 |
| B、Al(OH)3 |
| C、Mg(OH)2 |
| D、NaHCO3 |
设NA表示阿伏加得德罗常数的数值,下列叙述正确的是( )
| A、NA个SO2分子的质量(以克为单位)与SO2的相对分子质量在数值上相同 |
| B、SO2的摩尔质量为64g |
| C、SO2的摩尔质量等于SO2的相对分子质量 |
| D、1 mol SO2 的质量为 64g/mol |
 ,其分子式为
,其分子式为