题目内容
科学工作者最近制造出第112号元素,其原子的质量数为277,这是迄今已知元素中最重的原子,关于该新元素的原子的下列叙述中正确的是( )
| A、其核内中子数112 |
| B、其原子质量是12C的277倍 |
| C、其核内中子数与质子数之差为53 |
| D、其原子核外的电子数为277 |
考点:质子数、中子数、核外电子数及其相互联系
专题:
分析:根据原子的原子序数=原子核内质子数=核外电子数=质量数-中子数分析解答.
解答:
解:A、因为112号新元素的原子序数是112,原子的原子序数=原子核内质子数=112,中子数=质量数-质子数=277-112=165,故A错误;
B、原子质量的质量之比=相对原子质量之比=原子的质量数之比,其原子质量与12C原子质量之比为277:12,故B错误;
C、质子数为112,中子数为165,则其核内中子数与质子数之差为53,故C正确;
D、原子的原子序数=原子核内质子数=核外电子数=112,故D错误.
故选C.
B、原子质量的质量之比=相对原子质量之比=原子的质量数之比,其原子质量与12C原子质量之比为277:12,故B错误;
C、质子数为112,中子数为165,则其核内中子数与质子数之差为53,故C正确;
D、原子的原子序数=原子核内质子数=核外电子数=112,故D错误.
故选C.
点评:本题考查了质量数、质子数、中子数之间的关系,难度不大,注意质子数决定元素种类,质量数决定核素种类.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
关于如图装置说法正确的是( )
A、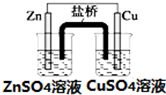 装置中,盐桥中的K+移向ZnSO4溶液 |
B、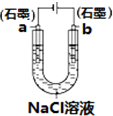 装置工作一段时间后,a极附近溶液的OH-的浓度增大 |
C、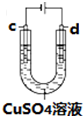 用装置精炼铜时,c极为粗铜 |
D、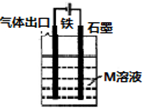 装置中若M是海水,该装置是通过“牺牲阳极保护法”使铁不被腐蚀 |
设NA表示阿伏加德罗常数的值.下列说法正确的是( )
| A、1molNa2O2固体中含有的阴阳离子总数为4NA |
| B、标准状况下,11.2L四氯化碳中含有的C-CI键的个数为2NA |
| C、1L1 mol?L-1的NaClO溶液中含有ClO-的数目为NA |
| D、常温常压下,14g由N2与CO组成的混合气体含有的原子数目为NA |
下列实验操作能达到实验目的是( )
| A、用加热蒸发Na2CO3溶液的方法除去少量NaHCO3 |
| B、向含有少量Fe3+的CuSO4溶液中加入铜片除去Fe3+ |
| C、用加热的方法分离NH4Cl和碘固体混合物 |
| D、用二氧化锰区别10%的H2O2溶液和10%的稀盐酸 |
下列物质中含有共价键的离子化合物是( )
①MgF2 ②Na2O2 ③NaOH ④CO2 ⑤NH4Cl ⑥H2O2 ⑦N2.
①MgF2 ②Na2O2 ③NaOH ④CO2 ⑤NH4Cl ⑥H2O2 ⑦N2.
| A、②③④⑤ | B、②③⑤ |
| C、①②③⑤ | D、①③⑤⑥ |
化学科学需要借助化学专用语言描述,下列有关化学用语正确的是( )
| A、乙炔的结构简式:CHCH |
| B、乙酸乙酯的实验式C4H8O2 |
C、一氯甲烷的电子式: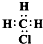 |
D、丙烷的球棍模型: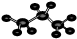 |
下列有关物质分类正确的是( )
①混合物:盐酸、铝热剂、纯碱、水银 ②化合物:CaCl2、烧碱、盐酸、HD
③电解质:H2SO4、胆矾、冰醋酸、硫酸钡 ④同素异形体:C60、C70、金刚石、石墨.
①混合物:盐酸、铝热剂、纯碱、水银 ②化合物:CaCl2、烧碱、盐酸、HD
③电解质:H2SO4、胆矾、冰醋酸、硫酸钡 ④同素异形体:C60、C70、金刚石、石墨.
| A、①③ | B、②④ | C、②③ | D、③④ |
用氢气还原ag氧化铜,得到bg铜,则铜的相对原子质量为( )
A、
| ||
B、
| ||
C、
| ||
D、
|
