题目内容
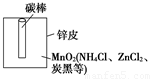
实验活动课上,学生从废旧干电池中回收碳棒、锌皮、二氧化锰、氯化铵、氯化锌等主要物质.(1)二氧化锰的作用是与正极上的产物(H2)反应,生成Mn2O3,写出该反应的化学方程式:______.
(2)得到氯化铵和氯化锌的晶体混合物后,检验其中含有NH4+的方法是______;
(3)学生将洗净的碳棒和锌皮堆放在一起晾干,一段时间后,发现锌皮上出现锈斑,用电极反应式阐明原因:______.
【答案】分析:(1)二氧化锰与H2反应,生成Mn2O3,根据电子注意守恒,氢气被氧化生成水;
(2)根据铵盐与碱反应生成氨气,利用氨气是碱性气体,能使湿润的红色石蕊试纸变蓝,据此检验NH4+;
(3)碳棒和锌皮与水膜构成原电池,发生吸氧腐蚀.
解答:解:(1)二氧化锰与H2反应,生成Mn2O3,根据电子注意守恒,氢气被氧化生成水,反应方程式为:2MnO2+H2=Mn2O3+H2O,
故答案为:2MnO2+H2=Mn2O3+H2O;
(2)检验其中含有NH4+的方法是;取少量晶体溶于NaOH溶液,加热,将湿润的红色石蕊试纸置于试管口,若试纸变蓝,则说明晶体中含有NH4+,
故答案为:取少量晶体溶于NaOH溶液,加热,将湿润的红色石蕊试纸置于试管口,若试纸变蓝,则说明晶体中含有NH4+;
(3)碳棒和锌皮与水膜构成原电池,锌为负极,反应氧化反应:Zn→Zn2++2e-,碳棒为正极,氧气放电生成氢氧根,电极反应式为:O2+2H2O+4e-→4OH-,Zn发生吸氧腐蚀,
故答案为:负极:Zn→Zn2++2e-,正极:O2+2H2O+4e-→4OH-.
点评:本题考查常用化学用语、铵根离子检验、原电池等,难度不大,注意对基础知识的理解掌握.
(2)根据铵盐与碱反应生成氨气,利用氨气是碱性气体,能使湿润的红色石蕊试纸变蓝,据此检验NH4+;
(3)碳棒和锌皮与水膜构成原电池,发生吸氧腐蚀.
解答:解:(1)二氧化锰与H2反应,生成Mn2O3,根据电子注意守恒,氢气被氧化生成水,反应方程式为:2MnO2+H2=Mn2O3+H2O,
故答案为:2MnO2+H2=Mn2O3+H2O;
(2)检验其中含有NH4+的方法是;取少量晶体溶于NaOH溶液,加热,将湿润的红色石蕊试纸置于试管口,若试纸变蓝,则说明晶体中含有NH4+,
故答案为:取少量晶体溶于NaOH溶液,加热,将湿润的红色石蕊试纸置于试管口,若试纸变蓝,则说明晶体中含有NH4+;
(3)碳棒和锌皮与水膜构成原电池,锌为负极,反应氧化反应:Zn→Zn2++2e-,碳棒为正极,氧气放电生成氢氧根,电极反应式为:O2+2H2O+4e-→4OH-,Zn发生吸氧腐蚀,
故答案为:负极:Zn→Zn2++2e-,正极:O2+2H2O+4e-→4OH-.
点评:本题考查常用化学用语、铵根离子检验、原电池等,难度不大,注意对基础知识的理解掌握.

练习册系列答案
相关题目
 某学校设计了一节实验活动课,让学生从废
某学校设计了一节实验活动课,让学生从废
旧干电池回收碳棒、锌皮、![]() 、
、![]() 、
、![]() 等物质,
等物质,
整个实验过程如下,请回答有关问题。
(1)有关干电池的基本构造和工作原理。右图是干电池的
基本构造图。干电池工作时负极上的电极反应式子是 ,![]()
的作用是除去正极上的产物,本身生成Mn2O3,该反应的化学方程式是 。
锌皮和碳棒的回收。用钳子和剪子开回收的干电池的锌筒,将锌皮和碳棒取出,并用手刷刷洗干净,将电池内的黑色粉末移入小烧杯中。
氧化铵、氯化锌的提取、检验和分离。
如何从黑色粉末中提取![]() 和
和![]() 等晶体的混合物?写出简要的实验步骤。
等晶体的混合物?写出简要的实验步骤。
设计简单的实验证明所得晶体中含有![]() 和
和![]() [一直
[一直![]() 是两性氢氧化物且溶解于氨水],并且填写下列实验报告。
是两性氢氧化物且溶解于氨水],并且填写下列实验报告。
| 实验步骤 | 实验现象 | 实验结论 | 有关离子方程式 |
| (a) | |||
| (b) | (c) | 说明有 | (d) |
| (e) | (f) | 说明有 |
(a) ,(b) ,(c) ,(d) ,(e) ,(f) ,
(4)最后剩余的黑色残渣的主要成分是![]() ,还有炭黑和有机物等。可用灼烧的方法除去杂质,该实验中需要用到的主要仪器除酒精灯外有(写其中2中即可) 。
,还有炭黑和有机物等。可用灼烧的方法除去杂质,该实验中需要用到的主要仪器除酒精灯外有(写其中2中即可) 。