题目内容
20.pH=11的X、Y两种碱溶液各5mL,分别稀释至500mL,其pH随溶液体积(V)变化的关系如图所示,下列说法正确的是( )
| A. | 稀释后X溶液中水的电离程度比Y溶液中水的电离程度小 | |
| B. | 若X、Y是一元碱,等物质的量浓度的盐酸盐溶液,Y的pH大 | |
| C. | 若X、Y都是一元弱碱,则a的值一定大于9 | |
| D. | 完全中和X、Y两溶液时,消耗同浓度稀硫酸的体积:V(X)>V(Y) |
分析 pH=11的X、Y两种碱溶液稀释100倍后,pH都减小,碱性越强的碱,其pH变化越明显,Y减小的程度小于X,则说明X的碱性大于Y,以此解答该题.
解答 解:pH=11的X、Y两种碱溶液稀释100倍后,pH都减小,碱性越强的碱,其pH变化越明显,Y减小的程度小于X,则说明X的碱性大于Y,
A.稀释后X溶液pH小,对水的电离的抑制程度比Y小,则水的电离程度较大,故A错误;
B.Y碱性较弱,如盐酸反应后溶液水解呈酸性,如都为弱碱,则水解程度大于X,Y的pH较小,故B错误;
C.如为强碱,加水稀释100倍,pH为9,若X、Y都是一元弱碱,加水稀释100时,pH大于9,故C正确.
D.Y碱性较弱,等pH时,溶液浓度较大,消耗同浓度稀硫酸的体积较大,故D错误;
故选C.
点评 本题考查了弱碱稀释PH变化曲线,明确弱电解质电离特点是解本题关键,根据pH变化大小确定碱相对强弱,再结合离子水解程度来分析解答,题目难度中等.

练习册系列答案
 全能测控一本好卷系列答案
全能测控一本好卷系列答案
相关题目
10.下列离子方程式正确的是( )
| A. | 向沸水中滴加FeCl3溶液制备Fe(OH)3胶体:Fe3++3H2O$\frac{\underline{\;\;△\;\;}}{\;}$Fe(OH)3↓+3H+ | |
| B. | 以石墨作电极电解氯化铝溶液:2Cl-+2H2O$\frac{\underline{\;电解\;}}{\;}$2OH-+H2↑+Cl2↑ | |
| C. | AlCl3溶液中加入过量的浓氨水:Al3++4NH3•H2O═AlO2-+4NH4++2H2O | |
| D. | 等体积、等浓度的稀溶液Ba(OH)2与NH4HCO3稀溶液混合:Ba2++2OH-+NH4++HCO3-═BaCO3↓+NH3•H2O+H2O |
11.有机物分子内基团间的相互影响会导致物质化学性质的不同.下列各项事实不能说明上述观点的是( )
| A. | 苯酚与溴水常温可以反应,而苯与溴水不能反应 | |
| B. | 乙烯能发生加成反应,而乙烷不能发生加成反应 | |
| C. | 苯酚与氢氧化钠溶液可以反应,而乙醇不能与氢氧化钠溶液发生反应 | |
| D. | 甲苯能使酸性高锰酸钾溶液褪色,而乙烷不能使酸性高锰酸钾溶液褪色 |
8.将NO、CO2的混合气体通过装有足量Na2O2的容器后,再用干燥烧瓶收集得到的混合气体,然后倒立于水槽中,最后水充满整个烧瓶,称量Na2O2容器,发现增重28g,则NO的质量是( )
| A. | 14g | B. | 20g | C. | 26g | D. | 28g |
5.向一定量的盐酸中逐滴加入NaAlO2溶液,生成沉淀Al(OH)3的量随NaAlO2加入量的变化关系如图所示.则下列离子组在对应的溶液中一定能大量共存的是( )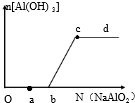

| A. | a点对应的溶液中:NH${\;}_{4}^{+}$、Fe3+、SO${\;}_{4}^{2-}$、HCO${\;}_{3}^{-}$ | |
| B. | b点对应的溶液中:K+、Na+、NO${\;}_{3}^{-}$、Cl- | |
| C. | c点对应的溶液中:Na+、K+、SO${\;}_{4}^{2-}$、OH- | |
| D. | d点对应的溶液中:Ca2+、NH4+、I-、H+ |
3.金属钨用途广泛,主要用于制造硬质或耐高温的合金,以及灯泡的灯丝.高温下,在密闭容器中用H2还原WO3可得到金属钨,其总反应为:WO3 (s)+3H2 (g)$\stackrel{高温}{?}$W (s)+3H2O (g)
请回答下列问题:
(1)上述反应的化学平衡常数表达式为$\frac{c{\;}^{3}(H{\;}_{2}O)}{c{\;}^{3}(H{\;}_{2})}$.
(2)某温度下反应达平衡时,H2与水蒸气的体积比为2:3,则H2的平衡转化率为60%;随温度的升高,H2与水蒸气的体积比减小,则该反应为吸热反应(填“吸热”或“放热”).
(3)上述总反应过程大致分为三个阶段,各阶段主要成分与温度的关系如下表所示:
第一阶段反应的化学方程式为2WO3+H2$\frac{\underline{\;高温\;}}{\;}$W2O5+H2O;580℃时,固体物质的主要成分为W2O5、WO2;假设WO3完全转化为W,则三个阶段消耗H2物质的量之比为1:1:4.
请回答下列问题:
(1)上述反应的化学平衡常数表达式为$\frac{c{\;}^{3}(H{\;}_{2}O)}{c{\;}^{3}(H{\;}_{2})}$.
(2)某温度下反应达平衡时,H2与水蒸气的体积比为2:3,则H2的平衡转化率为60%;随温度的升高,H2与水蒸气的体积比减小,则该反应为吸热反应(填“吸热”或“放热”).
(3)上述总反应过程大致分为三个阶段,各阶段主要成分与温度的关系如下表所示:
| 温度 | 25℃~550℃~600℃~700℃ |
| 主要成份 | WO3 W2O5 WO2 W |
1.下列反应的离子方程式中正确的是( )
| A. | 铜片插入硝酸银溶液中:Cu+Ag+=Cu2++Ag | |
| B. | 氢氧化钡溶液与稀硫酸混合:Ba2++OH-+H++SO42-=BaSO4↓+H2O | |
| C. | 澄清石灰水与Na2CO3溶液混合:Ca2++CO32-═CaCO3↓ | |
| D. | CaCO3与醋酸(CH3COOH)反应:CaCO3+2H+=Ca2++CO2↑+H2O |