��Ŀ����
ԭ���ԭ���ķ����Ǵ��ܺ��ܼ����ľ�������ǻ�ѧ�������һ���ش��ס�
��1����������������Ӧ��A��NaOH+HCl=NaCl+H2O��B��Zn+H2SO4=ZnSO4+H2��
�ж��ܷ���Ƴ�ԭ���A�� ��B�� ������ܡ����ܡ���
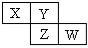
��2������пƬ�ʹ�ͭƬ��ͼ��ʽ����100 mL��ͬŨ�ȵ�ϡ������һ��ʱ�䣬�ش��������⣺

������˵����ȷ���� ��
A���ס��Ҿ�Ϊ��ѧ��ת��Ϊ���ܵ�װ��
B������ͭƬ��û�����Ա仯
C������ͭƬ�������١�����пƬ��������
D�����ձ�����Һ��pH������
������ͬʱ���ڣ����ձ��в������ݵ��ٶȣ��� �ң������������������ ��
����д��ͼ�й���ԭ��صĸ����缫��Ӧʽ ��
�ܵ����в���1��12L����״��������ʱ����п��ͭƬȡ�����ٽ��ձ��е���Һϡ����1 L�������Һ��c(H��)��0��1 mol��L��1���跴Ӧǰ����Һ������䣩����ȷ��ԭϡ��������ʵ���Ũ��Ϊ ��
��3��ȼ�ϵ�صĹ���ԭ���ǽ�ȼ�Ϻ�������(��O2)��Ӧ���ų��Ļ�ѧ��ֱ��ת��Ϊ���ܡ������һȼ�ϵ�أ��Ե缫aΪ�������缫bΪ����������Ϊȼ�ϣ���������������ҺΪ���Һ��������Ӧͨ�� ��(��a��b����ͬ)�����Ӵ� ��������
��1������ ��
��2����BD �ڣ� ��Zn - 2e- = Zn2+ ��1mol��L��1
��3��b b
��������
�����������1��A���ڸ��ֽⷴӦ������������ԭ��Ӧ�����Բ�����Ƴ�ԭ��أ�B���û���Ӧ����������ԭ��Ӧ������Ƴ�ԭ��ء���2����A���߱�ԭ����γɵ��������ܰѻ�ѧ��ת��Ϊ���ܣ����Ҳ��߱�ԭ����γɵ����������ܰѻ�ѧ��ת��Ϊ���ܡ�����B�����ڻ��Cu<H������Cu���ܰ����е����û���������ȷ��C������Zn������������������Ӧ���������٣�Cu���������缫�������μӷ�Ӧ������ͭƬ�������䣻����Zn���ڻ�Ա�Hǿ�����Կ��Ժ����ᷢ���û���Ӧ�������������пƬ�������١�����D�������ձ�������ϱ����ģ�c(H+)��С�������Һ��pH��������ȷ���������ڼ��ձ����γ���ԭ��أ����Լӿ컯ѧ��Ӧ���ʡ���������ͬʱ���ڣ����ձ��в������ݵ��ٶȣ��ף��ҡ����ڼ��ձ����γ���ԭ��أ������ĵ缫ʽΪZn - 2e- = Zn2+����n(H2)= 1��12L��22��4L/mol=0��05mol���������ĵ�H+�����ʵ���Ϊ0��1mol��n(H+)(��)=0��1mol+0��1 mol/L��1L=0��2mol������ԭ��Һ��c(H+)=0��2mol��0��1L=2mol/L��c(H2SO4)=1/2 c(H+)= 1mol/L����3��ͨ�������ĵ缫Ϊ������ͨ�������ĵ缫Ϊ�������������Ӧͨ��缫b������Ӧͨ��缫a�����ӴӸ���b���������뵽����b�缫��
���㣺����ԭ����γɵ�������ԭ��ط�Ӧ�Ի�ѧ��Ӧ���ʡ���Һ������ԵıȽϡ��缫��Ӧ�͵缫���жϵ�֪ʶ��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�