题目内容
某研究性学习小组查阅资料得知,漂白粉与硫酸溶液反应可制取氯气,化学方程式为:Ca(ClO)2+CaCl2+2H2SO4
| ||
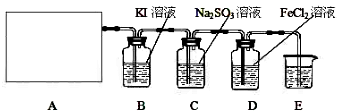
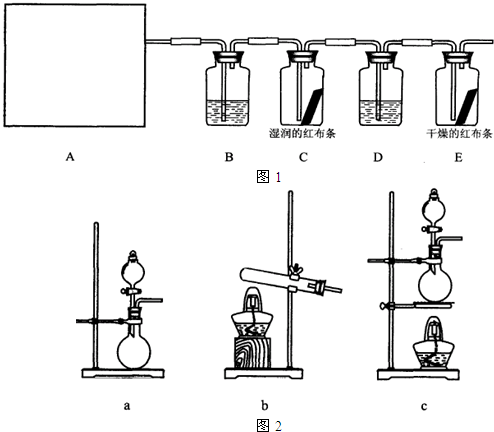
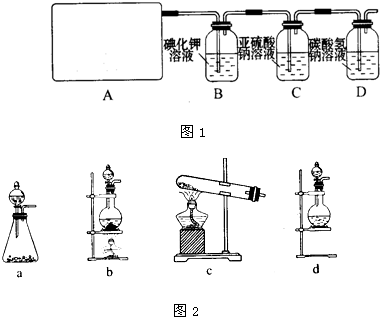
他们设计图1所示装置制取氯气并验证其性质.

试回答:
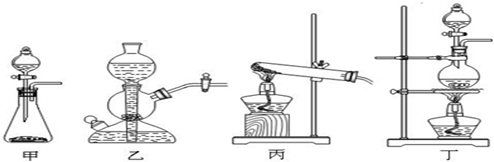
(1)该图1实验中A部分的装置是(如图2)
(2)A中发生反应一段时间后,B中的现象是
(3)请你帮助他们设计一个实验,证明洗气瓶C中的Na2SO3已被氧化(简述实验步骤)
(4)写出D装置中发生反应的离子方程式
分析:(1)根据反应物的状态及反应条件选择气体的发生装置;
(2)氯气具有强的氧化性,与碘化钾反应生成单质碘和氯化钾,单质碘遇淀粉变蓝;氯气是有毒的气体,不能直接排放到空气中,要用尾气处理装置处理;
(3)亚硫酸钠被氧化生成硫酸钠,只有验证硫酸根离子的存在就可证明亚硫酸钠已经被氧化;
(4)氯气溶于水和水反应生成盐酸和次氯酸,盐酸和碳酸氢钠反应生成水和二氧化碳.
(2)氯气具有强的氧化性,与碘化钾反应生成单质碘和氯化钾,单质碘遇淀粉变蓝;氯气是有毒的气体,不能直接排放到空气中,要用尾气处理装置处理;
(3)亚硫酸钠被氧化生成硫酸钠,只有验证硫酸根离子的存在就可证明亚硫酸钠已经被氧化;
(4)氯气溶于水和水反应生成盐酸和次氯酸,盐酸和碳酸氢钠反应生成水和二氧化碳.
解答:解:(1)从方程式可知反应物是固体和液体,反应条件是加热,所以应选固液混合加热型装置,
故答案为:b;
(2)氯气具有强的氧化性,碘化钾反应2KI+Cl2═2KCl+I2,生成的I2遇到淀粉变蓝色;氯气是有毒的气体,不能直接排放到空气中,要用尾气处理装置处理;
故答案为:溶液变成蓝色;2KI+Cl2═2KCl+I2;无尾气吸收;
(3)亚硫酸钠被氧化生成硫酸钠,只有验证硫酸根离子的存在就可证明亚硫酸钠已经被氧化,检验硫酸根离子的存在选用试剂稀盐酸和氯化钡溶液,实验设计如下:取少量溶液置于洁净试管中,向其中加入稀盐酸至不再产生气体,再向其中滴入氯化钡溶液,若产生白色沉淀证明Na2SO3已被氧化;
故答案为:取少量溶液置于洁净试管中,向其中加入稀盐酸至不再产生气体,再向其中滴入氯化钡溶液,若产生白色沉淀证明Na2SO3已被氧化;
(4)D装置中发生两个反应:氯气和水反应、盐酸和碳酸氢钠,反应的离子方程式分别为:Cl2+H2O═H++Cl-+HClO,H++HCO3-═H2O+CO2↑,
故答案为:Cl2+H2O═H++Cl-+HClO,H++HCO3-═H2O+CO2↑.
故答案为:b;
(2)氯气具有强的氧化性,碘化钾反应2KI+Cl2═2KCl+I2,生成的I2遇到淀粉变蓝色;氯气是有毒的气体,不能直接排放到空气中,要用尾气处理装置处理;
故答案为:溶液变成蓝色;2KI+Cl2═2KCl+I2;无尾气吸收;
(3)亚硫酸钠被氧化生成硫酸钠,只有验证硫酸根离子的存在就可证明亚硫酸钠已经被氧化,检验硫酸根离子的存在选用试剂稀盐酸和氯化钡溶液,实验设计如下:取少量溶液置于洁净试管中,向其中加入稀盐酸至不再产生气体,再向其中滴入氯化钡溶液,若产生白色沉淀证明Na2SO3已被氧化;
故答案为:取少量溶液置于洁净试管中,向其中加入稀盐酸至不再产生气体,再向其中滴入氯化钡溶液,若产生白色沉淀证明Na2SO3已被氧化;
(4)D装置中发生两个反应:氯气和水反应、盐酸和碳酸氢钠,反应的离子方程式分别为:Cl2+H2O═H++Cl-+HClO,H++HCO3-═H2O+CO2↑,
故答案为:Cl2+H2O═H++Cl-+HClO,H++HCO3-═H2O+CO2↑.
点评:本题考查氯气的实验室制备、氯气的性质、实验的设计,硫酸根离子的检验注意排除其他离子的干扰.

练习册系列答案
相关题目