题目内容
某温度下在密闭容器中发生如下反应3 M(g)+ N(g) 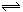 2G(g)
2G(g)
若开始时只充入2molG(g),达平衡时,混合气体的压强比起始时增加20%,若开始时只充入3 molM和1molN的混合气体,达平衡时M的转化率为
A.20% B.40% C.60% D. 80%
D
【解析】
试题分析:因为平衡的建立和途径无关,2molG(g)就相当于是2molM和1molN,即平衡是等效的。
2M(g)+ N(g)  2G(g)
2G(g)
起始量(mol) 0 0 2
转化量(mol) 2x x 2x
平衡量(mol) 2x x 2-2x
压强之比是物质的量之比
所以有
解得x=0.4
所以在平衡体系中M的物质的量是0.8mol
因此其转化率是
答案选C。
考点: 等效平衡和化学平衡计算。

分析下表中的四个热化学方程式,判断氢气和丙烷的燃烧热分别是
“嫦娥一号”发射火箭燃料 | 液氢(H2) | ①2H2(g)+O2(g) ②2H2 (l)+O2(l) |
北京奥运“祥云”火炬燃料 | 丙烷 (C3H8) | ③C3H8 (l)+5O2(g) ④C3H8(g)+5O2(g) |
A.571.6 kJ·mol-1,2 221.5 kJ·mol-1
B.241.3 kJ·mol-1,2 013.8 kJ·mol-1
C.285.8 kJ·mol-1,2 013.8 kJ·mol-1
D.285.8 kJ·mol-1,2 221.5 kJ·mol-1

 2H2O(l) ΔH=-571.6 kJ·mol-1
2H2O(l) ΔH=-571.6 kJ·mol-1 不变
不变