题目内容
把锌片和铁片放在盛有稀食盐和酚酞混合液的U形管中,如下图所示,最终可在A极观察到酚酞变红。A是原电池的正极还是负极?是锌还是铁?写出电极反应和总反应式。
____________________________________________________________

解析:这个装置是原电池,Zn作原电池的负极,Fe作正极,负极发生氧化反应:Zn-2e-![]() Zn2+,正极上发生还原反应:2H2O+O2+4e-
Zn2+,正极上发生还原反应:2H2O+O2+4e-![]() 4OH-,所以正极附近OH-浓度变大,使酚酞变红。?
4OH-,所以正极附近OH-浓度变大,使酚酞变红。?
答案:A是正极,Fe作正极材料。?
负极:2Zn-4e-![]() 2Zn2+?
2Zn2+?
正极:O2+4e-+2H2O![]() 4OH-?
4OH-?
总反应:2Zn+O2+2H2O![]() 2Zn(OH)2
2Zn(OH)2

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
把锌片和铁片放在盛有食盐水和酚酞的表面皿中,如图所示。
最先观察到酚酞变红的现象的区域是
| A.I和III | B.I和IV |
| C.II和III | D.II和IV |
把锌片和铁片放在盛有稀食盐水和酚酞试液混合溶液的玻璃皿中(如图所示平面图),经过一段时间后,两个实验中,首先观察到溶液变红的区域是( )
| A.Ⅰ和Ⅲ附近 | B.Ⅰ和Ⅳ附近 | C.Ⅱ和Ⅲ附近 | D.Ⅱ和Ⅳ附近 |
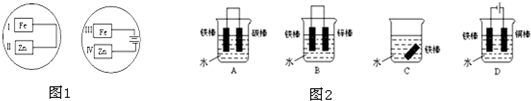
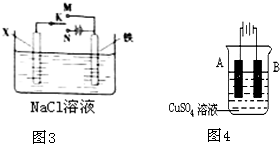
 把锌片和铁片放在盛有稀食盐水和酚酞试液混合溶液的玻璃皿中(如图所示平面图),经过一段时间后,首先观察到溶液变红的区域是( )
把锌片和铁片放在盛有稀食盐水和酚酞试液混合溶液的玻璃皿中(如图所示平面图),经过一段时间后,首先观察到溶液变红的区域是( )