题目内容
向10mL2mol/L的氯化铝溶液中加入0.5mol/L的烧碱溶液,反应得到沉淀0.78g,则加入的烧碱溶液的体积为
A.30mL B.60mL C.90mL D.140mL
BD
【解析】
试题分析:氯化铝的物质的量为0.01L×2mol/L=0.02mol,若全部转化为沉淀时生成沉淀的质量为0.02×78=1.56g,实际上反应得到沉淀0.78g,即0.01mol,说明有两种情况,①氢氧化钠不够,氯化铝一部分生成氢氧化铝,根据Al3++3OH-=Al(OH)3 ,消耗烧碱溶液的体积为0.3/0.5=0.6L=60mL;②氢氧化钠部分过量,根据Al3++3OH-=Al(OH)3、Al3+ +4OH- =[Al(OH)4]- ,消耗烧碱的体积是(0.3+0.4)/0.5=0.12L=120mL,选BD。
考点:考查铝的化合物的化学性质。

 千里马走向假期期末仿真试卷寒假系列答案
千里马走向假期期末仿真试卷寒假系列答案(14分)实验室制取乙酸丁酯的实验装置有如右下图所示两种装置供选用。其有关物质的物理性质

如下表:
乙酸 | 1-丁醇 | 乙酸丁酯 | |
熔点(℃) | 16.6 | -89.5 | -73.5 |
沸点(℃) | 117.9 | 117 | 126.3 |
密度(g/cm3) | 1.05 | 0.81 | 0.88 |
水溶性 | 互溶 | 可溶(9g/100g水) | 微溶 |
(1)制取乙酸丁酯的装置应选用_______(填“甲”或“乙”)。不选另一种装置的理由是 。
(2)该实验生成物中除了主产物乙酸丁酯外,还可能生成的有机副产物有(写出结构简式): 、 。
(3)酯化反应是一个可逆反应,为提高1-丁醇的利用率,可采取的措施是 。
(4)从制备乙酸丁酯所得的混合物中分离、提纯乙酸丁酯时,需要经过多步操作,下列图示的操作中,肯定需要的化学操作是__________(选填答案编号)。

(5)有机物的分离操作中,经常需要使用分液漏斗等仪器。使用分液漏斗前必须 ;某同学在进行分液操作时,若发现液体流不下来,其可能原因除分液漏斗活塞堵塞外,还可能 。
下列有关实验设计或操作、观察或记录、结论或解释都正确的是
实验设计或操作 | 观察或记录 | 结论或解释 | |
A | 将少量浓硝酸分多次加入Cu和稀硫酸的混合液中 | 产生红棕色气体 | 硝酸的还原产物是NO2 |
B | 某粉末用酒精润湿后,用铂丝蘸取做焰色反应 | 火焰呈黄色 | 该粉末一定不含钾盐 |
C | 在A1C13 和MgCl2 的混合液中加入过量NaOH溶液 | 先生成白色沉淀,后沉淀部分溶解 | 金属性Na>Mg>Al |
D | 将盛水的分液漏斗先静置,再倒置 | 漏斗口和活塞不渗水 | 分液漏斗不漏液 |

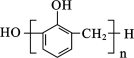
 它可以发生酯化、水解、加成等反应
它可以发生酯化、水解、加成等反应