题目内容
【题目】过硫酸钠(Na2S2O8)具有极强的氧化性,且不稳定,某化学兴趣小组探究过硫酸钠的相关性质,实验如下。已知SO3是无色易挥发的固体,熔点16.8℃,沸点44.8℃。
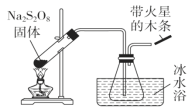
(1)稳定性探究(装置如图):
分解原理:2Na2S2O8![]() 2Na2SO4+2SO3↑+O2↑。
2Na2SO4+2SO3↑+O2↑。
此装置有明显错误之处,请改正:______________________,水槽冰水浴的目的是____________________;带火星的木条的现象_______________。
(2)过硫酸钠在酸性环境下,在Ag+的催化作用下可以把Mn2+氧化为紫红色的离子,所得溶液加入BaCl2可以产生白色沉淀,该反应的离子方程式为______________________,该反应的氧化剂是______________,氧化产物是________。
(3)向上述溶液中加入足量的BaCl2,过滤后对沉淀进行洗涤的操作是___________________________。
(4)可用H2C2O4溶液滴定产生的紫红色离子,取20mL待测液,消耗0.1mol·L-1的H2C2O4溶液30mL,则上述溶液中紫红色离子的浓度为______mol·L-1,若Na2S2O8有剩余,则测得的紫红色离子浓度将________(填“偏高”“偏低”或“不变”)。
【答案】试管口应该略向下倾斜 冷却并收集SO3 木条复燃 2Mn2++5S2O![]() +8H2O
+8H2O![]() 2MnO
2MnO![]() +10SO
+10SO![]() +16H+ S2O
+16H+ S2O![]() MnO 用玻璃棒引流,向漏斗中加蒸馏水至没过沉淀,使蒸馏水自然流下,重复操作2~3次(合理即可) 0.06 偏高
MnO 用玻璃棒引流,向漏斗中加蒸馏水至没过沉淀,使蒸馏水自然流下,重复操作2~3次(合理即可) 0.06 偏高
【解析】
(1)在试管中加热固体时,试管口应略微向下倾斜;根据SO3、氧气的性质进行分析;
(2)X为MnO4-,向所得溶液中加入BaCl2溶液可以产生白色沉淀,则产物中有SO42-,据此写出离子方程式,并根据氧化还原反应规律判断氧化剂、氧化产物;
(3)根据沉淀洗涤的方法进行回答;
(4)根据得失电子守恒可得到关系式:5H2C2O4---2MnO4-,带入数值进行计算;Na2S2O8也具有氧化性,氧化H2C2O4。
(1)在试管中加热固体时,试管口应略微向下倾斜,SO3的熔、沸点均在0℃以上,因此冰水浴有利于将SO3冷却为固体,便于收集SO3,由Na2S2O8的分解原理可知,生成物中有氧气,所以在导管出气口的带火星的木条会复燃,故答案为:试管口应该略向下倾斜;冷却并收集SO3;木条复燃;
(2)X为MnO4-,向所得溶液中加入BaCl2溶液可以产生白色沉淀,则产物中有SO42-,则反应的离子方程式为2Mn2++5S2O![]() +8H2O
+8H2O![]() 2MnO
2MnO![]() +10SO
+10SO![]() +16H+,根据该反应中元素化合价的变化可知,氧化剂是S2O82-,氧化产物是MnO4-,故答案为:2Mn2++5S2O
+16H+,根据该反应中元素化合价的变化可知,氧化剂是S2O82-,氧化产物是MnO4-,故答案为:2Mn2++5S2O![]() +8H2O
+8H2O![]() 2MnO
2MnO![]() +10SO
+10SO![]() +16H+;S2O82-;MnO4-;
+16H+;S2O82-;MnO4-;
(3)沉淀洗涤时,需要用玻璃棒引流,并且所加蒸馏水需要没过沉淀,需要洗涤2~3次,故答案为:用玻璃棒引流,向漏斗中加蒸馏水至没过沉淀,使蒸馏水自然流下,重复操作2~3次(合理即可);
(4)根据得失电子守恒可得到关系式:

则![]() ,Na2S2O8具有氧化性,消耗的H2C2O4溶液增多,导致测得的结果偏高,故答案为:0.06;偏高。
,Na2S2O8具有氧化性,消耗的H2C2O4溶液增多,导致测得的结果偏高,故答案为:0.06;偏高。

 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案【题目】《我在故宫修文物》展示了专家精湛的技艺和对传统文化的热爱与坚守,也令人体会到化学方法在文物保护中的巨大作用,某博物馆修复出土铁器的过程如下:
(1)检测锈蚀产物
主要成分的化学式 | |||
|
|
|
|
铁器在具有![]() 、_____等环境中容易被腐蚀。
、_____等环境中容易被腐蚀。
(2)分析腐蚀原理:一般认为,铁经过了如下腐蚀循环。
Ⅰ.![]() 转化为
转化为![]() 。
。
Ⅱ.![]() 在自然环境中形成
在自然环境中形成![]() ,该物质中铁元素的化合价为_______。
,该物质中铁元素的化合价为_______。
Ⅲ.![]() 和
和![]() 反应形成致密的
反应形成致密的![]() 保护层,
保护层,![]() 的作用是_______。
的作用是_______。
a.氧化剂 b.还原剂 c.既不是氧化剂也不是还原剂
Ⅳ.![]() 保护层被氧化为
保护层被氧化为![]() ,如此往复腐蚀,___
,如此往复腐蚀,___![]() +___
+___![]() +___
+___![]()
![]() ____
____![]() (将反应补充完整)
(将反应补充完整)
(3)研究发现,Cl-对铁的腐蚀会造成严重影响。化学修复:脱氯、还原,形成![]() 保护层,法如下: 将铁器浸没在盛有
保护层,法如下: 将铁器浸没在盛有![]() 溶液的容器中,缓慢加热至 60~90℃。一段时间, 取出器物,用
溶液的容器中,缓慢加热至 60~90℃。一段时间, 取出器物,用![]() 溶液洗涤至无Cl-。
溶液洗涤至无Cl-。
①检测洗涤液中 Cl-的方法是_____。
②脱氯反应:![]() 。离子反应的本质是离子浓度的减小,比较
。离子反应的本质是离子浓度的减小,比较![]() 与
与![]() 溶解度的大小:__________较大。[填
溶解度的大小:__________较大。[填![]() 与
与![]() ]
]