题目内容
3.(1)请把符合要求的化学方程式的编号填在下列空白处:①既属于分解反应又是氧化还原反应的是D.
②属于化合反应,但不是氧化还原反应的是E.
③既属于化合反应,又是氧化还原反应的是B.
④属于分解反应,但不是氧化还原反应的是A.
A.2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑
B.2Na+Cl2$\frac{\underline{\;点燃\;}}{\;}$2NaCl
C.Zn+CuSO4═ZnSO4+Cu
D.2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑
E.CaO+CO2═CaCO3
F.4FeS2+11O2$\frac{\underline{\;高温\;}}{\;}$2Fe2O3+8SO2
(2)根据反应Cu+4HNO3(浓)═Cu(NO3)2+2NO2↑+2H2O,回答下列问题:
①还原剂是Cu,还原产物是NO2.
②氧化剂与氧化产物的物质的量比是2:1.
③当有2mol HNO3参加反应时,被氧化的物质是32g.
分析 (1)氧化还原反应的特征是元素化合价的升降,如有元素化合价的变化,则属于氧化还原反应,结合分解反应和化合反应的特点解答该题;
(2)Cu+4HNO3(浓)═Cu(NO3)2+2NO2↑+2H2O中,Cu元素的化合价升高,N元素的化合价降低,结合元素的化合价变化及反应计算解答.
解答 解:(1)A.2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑
B.2Na+Cl2$\frac{\underline{\;点燃\;}}{\;}$2NaCl
C.Zn+CuSO4═ZnSO4+Cu
D.2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑
E.CaO+CO2═CaCO3
F.4FeS2+11O2$\frac{\underline{\;高温\;}}{\;}$2Fe2O3+8SO2
A.2NaHCO3$\frac{\underline{\;\;△\;\;}}{\;}$Na2CO3+H2O+CO2↑,为分解反应,但化合价没有发生变化,则不是氧化还原反应;
B.2Na+Cl2$\frac{\underline{\;点燃\;}}{\;}$2NaCl,为化合反应,Cl和Na元素化合价发生变化,属于氧化还原反应;
C.Zn+CuSO4═ZnSO4+Cu,为置换反应,Cu和Zn元素化合价发生变化,属于氧化还原反应;
D.2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,属于分解反应,Mn和O元素化合价发生变化,属于氧化还原反应;
E.CaO+CO2═CaCO3,为化合反应,元素化合价没有发生变化,不是氧化还原反应,
F.4FeS2+11O2$\frac{\underline{\;高温\;}}{\;}$2Fe2O3+8SO2,元素化合价发生变化,是氧化还原反应,但不属于分解和化合反应;
故答案为:①D;②E;③B;④A;
(2)①Cu失去电子被氧化,则Cu为还原剂,N得到电子被还原,则NO2为还原产物,故答案为:Cu;NO2;
②Cu元素的化合价升高,N元素的化合价降低,则HNO3为氧化剂,Cu为还原剂,且反应中HNO3一半作氧化剂,由反应可知氧化剂与还原剂的物质的量之比是2:1,
故答案为:2:1;
③当有2mol HNO3参加反应时,被氧化的物质是Cu,其质量为2mol×$\frac{1}{4}$×64g/mol=32g,故答案为:32.
点评 本题考查氧化还原反应,侧重于学生的分析能力考查,为高频考点,注意从元素化合价的角度认识氧化还原反应的相关概念和物质的性质,把握物质的反应类型和,难度不特点的判断,难度不大.

| 氧化剂 | 还原剂 | 其他反应物 | 氧化产物 | 还原产物 | |
| ① | Cl2 | FeBr3 | Cl- | ||
| ② | KMnO4 | H2O2 | H2SO4 | Cl2 | Mn2+ |
| ③ | KClO3 | 浓盐酸 | O2 |
| A. | 表中①组反应可能有一种或两种元素被氧化 | |
| B. | 表中②组反应的离子方程式是2MnO4-+3H2O2+6H+═2Mn2++4O2↑+6H2O | |
| C. | 表中③组反应的还原产物是KC1,电子转移数目是6e- | |
| D. | 氧化性强弱比较:KClO3>Fe3+>Cl2>Br2 |
| A. | 电解质溶液导电的过程实际上就是电解的过程 | |
| B. | 利用电解饱和食盐水所得的产物可以生产盐酸 | |
| C. | 氢氧燃料电池的负极通入的是氢气 | |
| D. | 铜在酸性环境中易发生析氢腐蚀 |
| A. | 苛性钠 | B. | 碱石灰 | C. | 盐酸 | D. | 铝 |
| A. | 容量瓶、量筒和滴定管上都标有使用温度,量筒、容量瓶无“0”刻度,滴定管有“0”刻度;使用时滴定管水洗后还需润洗,但容量瓶水洗后不用润洗 | |
| B. | 用电子天平称量化学药品时,必须先称小烧杯的质量,再称量加入试剂后的总质量,两者之差即为药品的质量 | |
| C. | 金属着火时,可用细沙覆盖灭火;电器设备引起的火灾,可用泡沫灭火器灭火 | |
| D. | 在酚酞溶液中加入过氧化钠粉末,溶液颜色会先变红后褪色,并且有气泡生成 |
①纯铁较生铁不易生锈;
②冶炼铝和钠都可以用电解法;
③KSCN溶液可以检验Fe3+离子;
④缺钙会引起骨质疏松,缺铁会引起贫血;
⑤青铜、不锈钢、硬铝都是合金;
⑥铜与硫反应,生成黑色的CuS.
| A. | ①②③④⑤ | B. | ②③④⑤⑥ | C. | ①③④⑤ | D. | ①②③④⑤⑥ |
| A. | 钠与水剧烈反应,反应产生的热量导致苯燃烧 | |
| B. | 钠在水层中反应并四处游动,并且发出“啪啪啪”的声音 | |
| C. | 钠在苯的液面上反应并四处游动 | |
| D. | 钠在苯与水的界面处反应并可能作上、下跳动 |
 阿司匹林是常用的解热镇痛剂,结构简式如图:
阿司匹林是常用的解热镇痛剂,结构简式如图: .
. ,合成M的流程图如下:
,合成M的流程图如下:


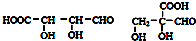 .
.