题目内容
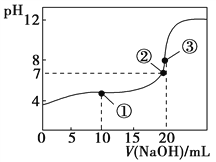
【题目】已知![]() 是二元弱酸,室温下向某浓度的草酸溶液中逐滴加入KOH溶液,所得溶液中
是二元弱酸,室温下向某浓度的草酸溶液中逐滴加入KOH溶液,所得溶液中![]() 、
、![]() 、
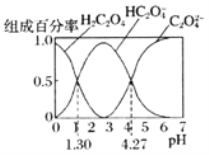
、![]() 的组成百分率与pH的关系如图所示:下列说法正确的是
的组成百分率与pH的关系如图所示:下列说法正确的是![]()
A.![]() 的溶液中:
的溶液中: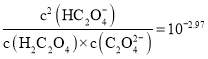
B.![]() 的溶液中,
的溶液中,![]()
C.反应![]() 的平衡常数为
的平衡常数为![]()
D.向溶液中加KOH溶液将pH由![]() 增大至
增大至![]() 的过程中水的电离程度先增大后减小
的过程中水的电离程度先增大后减小
【答案】B
【解析】
图象反应是溶液中的平衡浓度下,pH与溶液中各组分浓度之间的关系,根据图象分析,![]() 时,
时,![]() ,草酸的一级解离常数为
,草酸的一级解离常数为 ,则
,则![]() ,
,![]() 时,
时,![]() ,草酸的二级解离常数为
,草酸的二级解离常数为 ,则
,则![]() ,
,
A.![]() 的溶液中,根据图象,此时
的溶液中,根据图象,此时![]() 占绝大部分,则
占绝大部分,则 的值必然大于1,应为
的值必然大于1,应为![]() ,选项A错误;
,选项A错误;
B.![]() 的溶液中,
的溶液中,![]() ,几乎不存在
,几乎不存在![]() ,根据电荷守恒,
,根据电荷守恒,![]() ,由于
,由于![]() ,则
,则![]() ,选项B正确;
,选项B正确;
C.反应![]() 为
为![]() 的水解反应,平衡常数为
的水解反应,平衡常数为 ,选项C错误;
,选项C错误;
D.向溶液中加KOH溶液,pH由![]() 增大至
增大至![]() 的过程中,溶液始终是酸性的,水的电离受到抑制,随着pH的增加,溶液中酸电离出的
的过程中,溶液始终是酸性的,水的电离受到抑制,随着pH的增加,溶液中酸电离出的![]() 越来越少,对水的抑制作用不断减弱,水的电离程度不断增大,选项D错误。
越来越少,对水的抑制作用不断减弱,水的电离程度不断增大,选项D错误。
答案选B。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目