题目内容
下列有关说法正确的是( )
| A、含有共价键的化合物一定是共价化合物 |
| B、分子中只有共价键的物质一定是共价化合物 |
| C、非金属元素不能组成离子化合物 |
| D、含有离子键的化合物一定是离子化合物 |
考点:共价键的形成及共价键的主要类型,离子化合物的结构特征与性质
专题:化学键与晶体结构
分析:含有离子键的化合物是离子化合物,离子化合物中可能含有共价键,只含共价键的化合物是共价化合物,共价化合物中一定不含离子键,以此解答.
解答:
解:A.部分离子化合物中也可能存在共价键,如NaOH等,故A错误;
B.由共价键形成的分子也可能为单质,如氧气等,故B错误;
C.非金属性元素可形成离子化合物,如铵盐,故C错误;
D.只有离子化合物含有离子键,故D正确.
故选D.
B.由共价键形成的分子也可能为单质,如氧气等,故B错误;
C.非金属性元素可形成离子化合物,如铵盐,故C错误;
D.只有离子化合物含有离子键,故D正确.
故选D.
点评:本题考查了化学键和物质的关系,明确共价键和离子键的区别,易错选项是C,注意铵盐全部由非金属性元素组成,为易错点.

练习册系列答案
 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案
相关题目
 某有机物的结构为图,该有机物不可能具有的性质是( )
某有机物的结构为图,该有机物不可能具有的性质是( )①可以燃烧氧化 ②能使酸性KMnO4溶液褪色 ③能跟NaOH溶液反应
④能发生分子内酯化反应 ⑤能发生加聚反应 ⑥它有手性碳原子
⑦能被催化氧化成醛.
| A、①④ | B、④⑥ | C、⑤⑦ | D、只有⑥ |
已知:
对于含Fe2(SO4)3、FeSO4和CuSO4各0.5mol的混合溶液1L,根据表中数据判断,下列说法错误的是( )
| 物质 | Fe(OH)2 | Cu(OH)2 | Fe(OH)3 |
| Ksp(25℃) | 8.0×10-16 | 2.2×10-20 | 4.0×10-38 |
| A、向混合溶液中逐滴加入NaOH溶液,最先看到红褐色沉淀 |
| B、向溶液中加入双氧水,并用CuO粉末调节pH,过滤后可获得溶质主要为CuSO4的溶液 |
| C、该溶液中c(SO42-):[c(Fe3+)+c(Fe2+)+c(Cu2+)]=5:4 |
| D、将少量FeCl3粉末加入含Cu(OH)2的悬浊液中,其中c(Cu2+)增大 |
某主族元素R原子的质量数为79,已知R离子含有45个中子和36个电子,下列关于R元素的叙述错误的是( )
| A、R元素属于ⅣA族 |
| B、R元素最高氧化物对应水化物的分子式为H2RO4 |
| C、R元素在周期表里处于第4周期 |
| D、R元素气态氢化物的分子式为H2R |
低温下蒸干下列溶液能得到原溶液中溶质的是( )
| A、AlCl3 |
| B、Cu(NO3)2 |
| C、Na2CO3 |
| D、(NH4)2S |
 某离子晶体晶胞结构如图所示,图中X位于立方体的顶点,Y位于立方体中心.晶体中距离最近的2个X与一个Y形成的夹角∠XYX的角度为( )
某离子晶体晶胞结构如图所示,图中X位于立方体的顶点,Y位于立方体中心.晶体中距离最近的2个X与一个Y形成的夹角∠XYX的角度为( )| A、109°28′ |
| B、107°18′ |
| C、90° |
| D、120 |
除去下列物质中所含少量杂质(括号内为杂质),所选用的试剂和分离方法能达到实验目的是( )
| 混合物 | 试剂 | 分离方法 | |
| A | 苯(苯酚) | 浓溴水 | 过滤 |
| B | 溴苯(Br2) | 苯 | 分液 |
| C | 乙醇(水) | Na | 蒸馏 |
| D | 甲烷(乙烯) | 溴水 | 洗气 |
| A、A | B、B | C、C | D、D |
下图是晶体结构中具有代表性的最小重复单元(晶胞)的排列方式,图中: -X、
-X、 -Y,
-Y, -Z.其对应的化学式不正确的是( )
-Z.其对应的化学式不正确的是( )
 -X、
-X、 -Y,
-Y, -Z.其对应的化学式不正确的是( )
-Z.其对应的化学式不正确的是( )A、 XY |
B、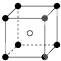 X2Y |
C、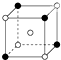 X3Y |
D、 XY3Z |
 S2Cl2广泛用于橡胶工业,其分子结构如图所示.常温下,S2Cl2遇水易水解,并产生能使品红褪色的气体.下列说法不正确的是( )
S2Cl2广泛用于橡胶工业,其分子结构如图所示.常温下,S2Cl2遇水易水解,并产生能使品红褪色的气体.下列说法不正确的是( )| A、S2Cl2与H2O反应的化学方程式为2S2Cl2+2H2O═SO2↑+3S↓+4HCl |
| B、S2Cl2分子中含有极性键和非极性键 |
| C、S2Br2与S2Cl2结构相似,熔、沸点:S2Br2>S2Cl2 |
| D、S2Cl2中S-S键键能大于S-Cl键 |