题目内容
对于物质的量相同的硫酸和磷酸(H3PO4),下列说法不正确的是( )
| A、原子总数不相同 |
| B、氧原子数相同 |
| C、分子数相同 |
| D、氢原子数相同 |
考点:物质的量的相关计算
专题:计算题
分析:A.一个硫酸分子中7个原子,一个磷酸分子中有8个原子;
B.一个硫酸分子中4个氧原子,一个磷酸分子中有4个氧原子;
C.分子数目之比等于其物质的量之比;
D.一个硫酸分子中2个氢原子,一个磷酸分子中有3个氢原子.
B.一个硫酸分子中4个氧原子,一个磷酸分子中有4个氧原子;
C.分子数目之比等于其物质的量之比;
D.一个硫酸分子中2个氢原子,一个磷酸分子中有3个氢原子.
解答:
解:A.一个硫酸分子中7个原子,一个磷酸分子中有8个原子,二者物质的量相同,含有原子总数之比为7:8,含有原子总数不相等,故A正确;
B.一个硫酸分子中4个氧原子,一个磷酸分子中有4个氧原子,二者物质的量相同,含有氧原子个数相同,故B正确;
C.根据N=nNA可知,二者物质的量相等,含有分子数目相等,故C正确;
D.一个硫酸分子中2个氢原子,一个磷酸分子中有3个氢原子,二者物质的量相同,含有H原子数目之比为2:3,含有氢原子数目不相等,故D错误,
故选D.
B.一个硫酸分子中4个氧原子,一个磷酸分子中有4个氧原子,二者物质的量相同,含有氧原子个数相同,故B正确;
C.根据N=nNA可知,二者物质的量相等,含有分子数目相等,故C正确;
D.一个硫酸分子中2个氢原子,一个磷酸分子中有3个氢原子,二者物质的量相同,含有H原子数目之比为2:3,含有氢原子数目不相等,故D错误,
故选D.
点评:本题考查微粒数目的计算,比较基础,注意对化学式意义的理解.

练习册系列答案
 活力课时同步练习册系列答案
活力课时同步练习册系列答案
相关题目
在相同条件下,2mL X(气)跟5mL C2(气)恰好完全反应,生成4mL AC2(气)与2mL B2C(气),则X的分子式是( )
| A、AB |
| B、B2C |
| C、A2B2 |
| D、BC2 |
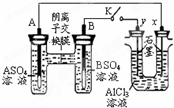 某同学按图所示的装置进行试验.A、B 为两种常见金属,它们的硫酸盐可溶于水.当 K 闭合时,在交换膜处 SO42-从右向左移动.下列分析错误的是( )
某同学按图所示的装置进行试验.A、B 为两种常见金属,它们的硫酸盐可溶于水.当 K 闭合时,在交换膜处 SO42-从右向左移动.下列分析错误的是( )| A、金属活动性A强于B |
| B、B电极反应B-2e-=B2+ |
| C、x电极上有H2产生,发生还原反应 |
| D、反应初期x 电极周围出现白色沉淀,继续实验沉淀将溶解 |
下列有关铝及其化合物的叙述正确的是( )
| A、铝粉与氧化镁共热可制取金属镁 |
| B、足量铝分别与含1 mol HCl、1 mol NaOH的溶液反应,产生相同量的氢气 |
| C、工业上用电解熔融Al2O3的方法冶炼铝 |
| D、在浓硝酸中加入等体积的浓硫酸后,立即加入铝片,铝片表面发生钝化 |
常温常压下,下列说法正确的是( )
| A、含有离子键的物质一定是离子化合物 |
| B、同素异形体之间的转化是物理变化 |
| C、含有共价键的物质一定是共价化合物 |
| D、气态物质,其微粒间一定存在共价键 |
当 15.6g Na2O2完全与CO2作用后,生成的O2的体积在标准状况下为( )
| A、2.24 L |
| B、4.48 L |
| C、11.2 L |
| D、22.4 L |
合成氨反应:3H2+N2?2NH3,其反应速率分别为v(H2),v(N2),v(NH3)(用mol?L-1?s-1表示),则正确的关系式是( )
| A、v(H2)=v(N2)=v(NH3) | ||
| B、v(N2)=2v(NH3) | ||
C、v(H2)=
| ||
| D、v(N2)=3v(H2) |
下列叙述正确的是( )
| A、久置在空气中的NaOH溶液,加盐酸时有气体产生 |
| B、50mL 12mol/L-1酸与足量的二氧化锰反应,都生成氯气0.15mol |
| C、在常温下,浓硫酸不与铜反应,是因为铜被钝化 |
| D、少量CO2通入浓的氯化钙溶液中有白色沉淀生成 |