题目内容
已知X、Y和Z为第三周期元素,其原子的第一至第四电离能如下表:
| 电离能/kJ·mol—1 | I1 | I2 | I3 | I4 |
| X | 578 | 1817 | 2745 | 11578 |
| Y | 738 | 1451 | 7733 | 10540 |
| Z | 496 | 4562 | 6912 | 9543 |
A.Z > Y > X B.X > Z > Y C.X > Y > Z D.Y > Z > X
C
解析试题分析:根据电离能的数据可知,X的第四电离能远大于第三电离能,所以X是第ⅢA元素;同样分析可知,Y是第ⅡA元素,而Z则是第IA元素。同周期元素自左向右非金属性逐渐增强,电负性也是逐渐增强的,所以答案选C。
考点:考查电离能和电负性的有关判断
点评:在一般情况下,非金属性越强,第一电离能和电负性都是逐渐增强的,但第一电离能有时会出现反常的。例如氮元素的第一电离能大于氧元素的,但电负性却小于氧元素的。

练习册系列答案
相关题目
已知X、Y和Z为第三周期元素,其原子的第一至第四电离能如下表:
则X、Y、Z的电负性从大到小的顺序为( )
| 电离能/kJ?mol-1 | I1 | I2 | I3 | I4 |
| X | 578 | 1817 | 2745 | 11578 |
| Y | 738 | 1451 | 7733 | 10540 |
| Z | 496 | 4562 | 6912 | 9543 |
| A、Z>Y>X |
| B、X>Z>Y |
| C、X>Y>Z |
| D、Y>Z>X |
常用于除去高速公路冰雪的是“氯盐类”融雪剂,如NaCl、MgCl2等,
请回答:
(1)“氯盐类”融雪剂主要成分的晶体类型为 ;
(2)冰比硫化氢熔点高的原因是 ,冰分子中氧原子的杂化轨道
类型为 ;水的密度在4℃最大的原因是 ;
(3)已知X、Y和Z为第三周期元素,其原子的第一至第四电离能如下表所示:
元素Y第一电离能大于X的原因是 ;
(4)已知CN-与 N2结构相似,1mol CN-中π键数目为 .
请回答:
(1)“氯盐类”融雪剂主要成分的晶体类型为
(2)冰比硫化氢熔点高的原因是
类型为
(3)已知X、Y和Z为第三周期元素,其原子的第一至第四电离能如下表所示:
| 电离能/kJ?mol-1 | I1 | I2 | I3 | I4 |
| X | 578 | 1817 | 2745 | 11578 |
| Y | 738 | 1451 | 7733 | 10540 |
| Z | 496 | 4562 | 6912 | 9543 |
(4)已知CN-与 N2结构相似,1mol CN-中π键数目为
 (2011?厦门一模)常用于除去高速公路冰雪的是“氧盐类”融雪剂,如NaCl、MgCl2等.请回答
(2011?厦门一模)常用于除去高速公路冰雪的是“氧盐类”融雪剂,如NaCl、MgCl2等.请回答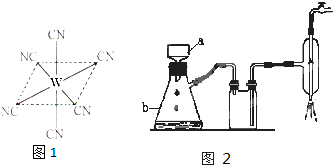
 常用于除去高速公路冰雪的是“氯盐类”融雪剂,如NaCl、MgCl2等,请回答:
常用于除去高速公路冰雪的是“氯盐类”融雪剂,如NaCl、MgCl2等,请回答: