题目内容
13.设NA为阿佛加德罗常数,下列说法正确的是( )①标准状况下,11.2L以任意比例混合的氮气和氧气所含的原子数为NA
②同温同压下,体积相同的氢气和氩气所含的分子数相等
③1L 2mol/L的氯化镁溶液中含氯离子为4NA
④标准状况下22.4LH2O中分子数为NA
⑤32g O2和O3混合气体中含有原子数为2NA.
| A. | ①②③④ | B. | ③④ | C. | ①③④ | D. | ①②③⑤ |
分析 ①氮气和氧气都是双原子分子,标况下11.2L混合气体的物质的量为0.5mol,含有1mol原子;
②相同条件下,等体积的任何气体含有的分子数一定相等;
③1L 2mol/L的氯化镁溶液中含氯离子为4NA;
④气体摩尔体积使用与气体;
⑤根据O2和O3均由氧原子构成来计算.
解答 解:①标准状况下,11.2L气体的物质的量为0.5mol,0.5mol氮气和氧气的混合气体中含有1mol原子,所含的原子数为NA,故正确;
②同温同压下,气体的摩尔体积相同,则体积相同的氢气和氩气的物质的量相同,所含的分子数相等,故正确;
③1L 2mol/L的氯化镁溶液中含氯离子为4NA,故正确;
④标准状况下,水不是气体,不能使用标况下的气体摩尔体积计算其物质的量,故错误;
⑤O2和O3均由氧原子构成,32gO2和O3含有的氧原子的物质的量n=$\frac{m}{M}$=$\frac{32g}{16g/mol}$=2mol,故含有原子数为2NA,故正确;
故选:D.
点评 本题考查阿伏加德罗常数的有关计算和判断,题目难度中等,注意明确标况下气体摩尔体积的使用条件,掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系是解题关键,题目难度不大.

练习册系列答案
相关题目
1.在0.5L的密闭容器中,一定量的氮气与氢气进行如下反应:N2(g)+3H2(g)?2NH3(g)△H=a kJ•mol-1,其化学平衡常数K与温度的关系如下.
请回答下列问题.
(1)写出该反应的化学平衡常数表达式:$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2})×{c}^{3}({H}_{2})}$,a小于(填“大于”、“小于”或“等于”)0.
(2)400℃时,2NH3(g)?N2(g)+3H2(g)的化学平衡常数为2,测得氨气、氮气、氢气的物质的量分别为3mol、2mol、1mol时,该反应的v正(N2)大于(填“大于”、“小于”或“等于”)v逆(N2),反应需向正方向进行才能达到新的平衡.
| 温度/℃ | 200 | 300 | 400 |
| K | 1.0 | 0.86 | 0.5 |
(1)写出该反应的化学平衡常数表达式:$\frac{{c}^{2}(N{H}_{3})}{c({N}_{2})×{c}^{3}({H}_{2})}$,a小于(填“大于”、“小于”或“等于”)0.
(2)400℃时,2NH3(g)?N2(g)+3H2(g)的化学平衡常数为2,测得氨气、氮气、氢气的物质的量分别为3mol、2mol、1mol时,该反应的v正(N2)大于(填“大于”、“小于”或“等于”)v逆(N2),反应需向正方向进行才能达到新的平衡.
8.溶液中,下列电离方程式正确的是( )
| A. | KAl (SO4)2=K++Al3++2 SO42- | B. | H2CO3=H++HCO3- | ||
| C. | Ca(HCO3)2=Ca2++2H++2CO32- | D. | Ba(OH)2=Ba2++OH2- |
18.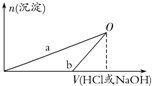 某同学研究铝及其化合物的性质时设计了如下两个实验方案.
某同学研究铝及其化合物的性质时设计了如下两个实验方案.
方案①:2.7g Al$\stackrel{100mLHCl}{→}$ X溶液$\stackrel{NaOH}{→}$Al(OH)3沉淀
方案②:2.7g Al$\stackrel{100mLNaOH}{→}$Y溶液$\stackrel{HCl}{→}$Al(OH)3沉淀
NaOH和HCl的浓度均是3mol/L,如图是向X溶液和Y溶液中分别加入NaOH和HCl时产生沉淀的物质的量与加入盐酸和氢氧化钠溶液体积之间的关系,下列说法不正确的是( )
 某同学研究铝及其化合物的性质时设计了如下两个实验方案.
某同学研究铝及其化合物的性质时设计了如下两个实验方案.方案①:2.7g Al$\stackrel{100mLHCl}{→}$ X溶液$\stackrel{NaOH}{→}$Al(OH)3沉淀
方案②:2.7g Al$\stackrel{100mLNaOH}{→}$Y溶液$\stackrel{HCl}{→}$Al(OH)3沉淀
NaOH和HCl的浓度均是3mol/L,如图是向X溶液和Y溶液中分别加入NaOH和HCl时产生沉淀的物质的量与加入盐酸和氢氧化钠溶液体积之间的关系,下列说法不正确的是( )
| A. | b曲线表示的是向X溶液中加入NaOH溶液 | |
| B. | 在O点时两方案中所得溶液浓度相等 | |
| C. | 方案②中对应的O点HCl恰好反应完 | |
| D. | X溶液显酸性,Y溶液显碱性 |
5.在离子方程式中,反应前后可以不相等的是( )
| A. | 原子总数 | B. | 离子总数 | C. | 电荷总数 | D. | 元素种类 |
3.LiOH是制备锂离子电池的材料,可由电解法制备.工业上利用如图装置电解制备LiOH,两电极区电解液分别为LiOH和LiCl溶液.下列说法正确的是( )

| A. | B极区电解液为LiCl溶液 | |
| B. | 电极每产生22.4L气体,电路中转移2mole- | |
| C. | 电解过程中Li+迁移入B电极区、OH-迁移入A电极区 | |
| D. | 电解池中总反应方程式为:2LiCl+2H2O$\frac{\underline{\;电解\;}}{\;}$H2↑+Cl2↑+2LiOH |
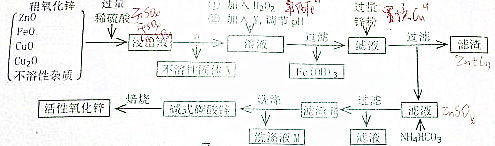
 如图所示,容器A左侧是可平行移动的活塞.向A中充入1molX和1molY,向B中充入2molX和2molY,起始时V(A)=V(B)=aL.在相同温度和有催化剂存在的条件下,两容器各自发生:X(g)+Y(g)?Z(g)+2W(g),达到平衡时V(A)=1.2aL.试回答:
如图所示,容器A左侧是可平行移动的活塞.向A中充入1molX和1molY,向B中充入2molX和2molY,起始时V(A)=V(B)=aL.在相同温度和有催化剂存在的条件下,两容器各自发生:X(g)+Y(g)?Z(g)+2W(g),达到平衡时V(A)=1.2aL.试回答:
 .
. .
. )是一种重要的有机合成中间体.试写出以苯、甲苯为原料制取该化合物的合成路线流程图(无机原料任选).合成路线流程图示例如下:
)是一种重要的有机合成中间体.试写出以苯、甲苯为原料制取该化合物的合成路线流程图(无机原料任选).合成路线流程图示例如下: .
.