题目内容
1.下列变化中生成物的总能量大于反应物的总能量的是( )| A. | 生石灰和水的反应 | B. | 木炭在氧气中发生不完全燃烧 | ||
| C. | 铝热反应 | D. | 氢氧化钡晶体与氯化铵晶体混合 |
分析 生成物的总能量大于反应物总能量说明反应是吸热反应;
根据常见的放热反应有:所有的物质燃烧、所有金属与酸反应、金属与水反应,所有中和反应;绝大多数化合反应和铝热反应;
常见的吸热反应有:绝大数分解反应,个别的化合反应(如C和CO2),少数分解置换以及某些复分解(如铵盐和强碱),C或氢气做还原剂时的反应.
解答 解:生成物的总能量大于反应物总能量说明反应是吸热反应,
A.生石灰和水的反应是放热反应,生成物总能量小于反应物总能量,故A错误;
B.木炭在氧气中的燃烧是放热反应,生成物总能量小于反应物总能量,故B错误;
C.铝热反应为放热反应,生成物总能量小于反应物总能量,故C错误;
D.氢氧化钡晶体与氯化铵晶体反应是吸热反应,生成物的总能量大于反应物的总能量,故D正确;
故选D.
点评 本题考查反应热与焓变的应用,题目难度不大,抓住中学化学中常见的吸热或放热的反应是解题的关键,对于特殊过程中的热量变化的要熟练记忆来解答此类习题.

练习册系列答案
 名师伴你成长课时同步学练测系列答案
名师伴你成长课时同步学练测系列答案
相关题目
12.下列叙述中正确的是( )
| A. | 使用含微量NaF的牙膏,可以使牙齿上的Ca5(PO4)3OH转化为Ca5(PO4)3F以防止蛀牙,则一般可说明后者的Ksp小于前者的Ksp | |
| B. | 室温下向苯和含少量苯酚杂质的混合溶液中加入适量浓溴水,振荡,静置后过滤,可除去苯中少量苯酚杂质 | |
| C. | 用1.00mol/L 标准盐酸滴定未知浓度的NaOH溶液10.00mL,滴定前将25.00mL 酸式滴定管中盐酸调至“0”刻度,将盐酸滴完恰好滴定至终点,则可得c(NaOH)=2.50mol/L | |
| D. | 向4ml 2%的CuSO4溶液中加入几滴1%的NaOH溶液,振荡后再加入0.5mL 有机物X,加热后未出现砖红色沉淀,说明X结构中不含有醛基 |
9.下列实验能达到实验目的是( )
| A. | 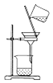 用装置分离Fe(OH)3胶体和NaCl溶液 | |
| B. | 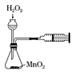 用装置定量测定H2O2的分解速率 | |
| C. |  用装置将CuSO4•5H2O变无水CuSO4 | |
| D. | 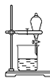 用装置④分离饱和Na2CO3溶液和CH3COOCH2CH3 |
16.下列气体不能用无水氯化钙干燥的是( )
| A. | H2 | B. | Cl2 | C. | NH3 | D. | CO2 |
6.下列关于铝热反应实验中涉及的化学方程式正确的是( )
| A. | 2Mg+O2$\frac{\underline{\;点燃\;}}{\;}$2MgO | B. | 2KClO3$\frac{\underline{\;\;△\;\;}}{\;}$2KCl+3O2↑ | ||
| C. | 3Mg+Fe2O3═3MgO+2Fe | D. | Al+Fe2O3═Al2O3+Fe |
7.标准状况下的甲烷和一氧化碳的混合气体8.96L,其质量为7.60g,则混合气体的物质的量为:0.4mol,平均摩尔质量为19g/mol;混合气体中甲烷的体积为6.72L;一氧化碳的质量为2.8g.
5.有机物a和苯通过反应合成b的过程可表示为图 (无机小分子产物略去).下列说法正确的是( )

| A. | 该反应是加成反应 | |
| B. | 若R为CH3时,b中所有原子可能共面 | |
| C. | 若R为C4H9时,取代b苯环上的氢的一氯代物的可能的结构共有12种 | |
| D. | 若R为C4H5O时,lmol b最多可以与6mol H2加成 |