题目内容
10.实验室可用如图所示的装置干燥、储存气体R,多余的气体可用水吸收,则R是( )
| A. | NO2 | B. | NO | C. | SO2 | D. | NH3 |
分析 根据装置特点可知:满足条件的气体的密度比空气小,且该气体极易溶于水,则选项中只有氨气符合条件.
解答 解:A.二氧化氮与水反应生成一氧化氮和硝酸,多余的气体不能用水吸收,且NO2密度大于空气的密度,采用集气瓶收集时应长进短出,故A错误;
B.NO的密度大于空气,集气瓶中的导气管应该采用长进短出的方式,且不能用水吸收多余的NO,故B错误;
C.SO2尾气须用碱性溶液吸收,SO2密度大于空气的密度,采用集气瓶收集时应长进短出,不符合图中装置要求,故C错误;
D.碱石灰能干燥NH3,NH3在水中的溶解度很大,所以能用水吸收多余的NH3,须用倒扣的漏斗防倒吸,故D正确;
故选D.
点评 本题考查实验装置的选择、气体的性质及收集、干燥方法,题目浓度中等,解答本题时既要考虑物质的水溶性,又要考虑气体的性质及收集方法,明确常见气体的性质为解答关键.

练习册系列答案
相关题目
14.已知:C(s)+2H2(g)→CH4(g)△H1
C(s)+$\frac{1}{2}$H2(g)→$\frac{1}{2}$C2H2(g)△H2
C(s)+H2(g)→$\frac{1}{2}$C2H4(g)△H3
C2H2(g)+H2(g)→C2H4(g)△H4=-26KJ•mol-1
$\frac{1}{2}$C2H4(g)+H2(g)→CH4(g)△H5=-20KJ•mol-1
下列关系正确的是( )
C(s)+$\frac{1}{2}$H2(g)→$\frac{1}{2}$C2H2(g)△H2
C(s)+H2(g)→$\frac{1}{2}$C2H4(g)△H3
C2H2(g)+H2(g)→C2H4(g)△H4=-26KJ•mol-1
$\frac{1}{2}$C2H4(g)+H2(g)→CH4(g)△H5=-20KJ•mol-1
下列关系正确的是( )
| A. | △H1>△H2 | B. | △H1>△H3 | C. | △H2>△H3 | D. | △H3>△H1>△H2 |
1.下列说法正确的是( )
| A. | 氯化铁溶液有较强氧化性,故可用作净水剂 | |
| B. | 煤中含有大量的有机物,用干馏的方法通过发生物理变化得到产物 | |
| C. | 除去CH4中的少量C2H4:通过盛有酸性高锰酸钾溶液的洗气瓶 | |
| D. | 将ag铜丝灼烧成黑色后趁热插入乙醇中,铜丝变红,再次称量质量等于a g |
18.下列溶液中,物质的量浓度最大的是( )
| A. | 将40 g NaOH溶于水并配成1 L的溶液 | |
| B. | 0.5 L含49 g H2SO4的溶液 | |
| C. | 将1mol Na2O 溶于水并配成1 L的溶液 | |
| D. | 含K+为1mol•L-1的K2SO4溶液 |
2.下列化合物中为离子化合物的是( )
| A. | CH4 | B. | O3 | C. | 盐酸 | D. | 氯化钾 |
20.下列关于燃料的说法错误的是( )
| A. | 煤可以气化得到发生炉煤气、水煤气、焦炉气,这些气体都含有CO | |
| B. | 液化石油气的成分不同于天然气,容易冒黑烟 | |
| C. | 沼气因使用具有危险性,不能推广使用 | |
| D. | 燃料电池能源的利用率高、污染少,具有很好的应用前景 |
 .
.
 ;名称是环己烷.
;名称是环己烷.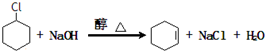 .
. +Br2→
+Br2→ .
. +2NaOH$→_{△}^{醇}$
+2NaOH$→_{△}^{醇}$ +2NaBr+2H2O.
+2NaBr+2H2O.