题目内容
下列物质不是电解质的是( )
| A、NaCl |
| B、H2SO4 |
| C、NaOH |
| D、SO3 |
考点:电解质与非电解质
专题:电离平衡与溶液的pH专题
分析:在水溶液里或熔融状态下能导电的化合物是电解质,电解质首先必须是化合物,酸、碱、盐、活泼金属氧化物、水属于电解质.
解答:
解:A、NaCl属于盐,溶于水能够电离出自由移动的阴阳离子而导电,属于电解质,故A不选;
B、硫酸属于强酸,溶于水能够电离出自由移动的阴阳离子而导电,属于电解质,故B不选;
C、NaOH属于强碱,溶于水能够电离出自由移动的阴阳离子而导电,属于电解质,故C不选;
D、SO3溶于水时本身不能电离出自由移动的阴阳离子,因此属于非电解质,故D选;
故选D.
B、硫酸属于强酸,溶于水能够电离出自由移动的阴阳离子而导电,属于电解质,故B不选;
C、NaOH属于强碱,溶于水能够电离出自由移动的阴阳离子而导电,属于电解质,故C不选;
D、SO3溶于水时本身不能电离出自由移动的阴阳离子,因此属于非电解质,故D选;
故选D.
点评:本题考查了电解质的判断,难度不大,电解质首先必须是化合物,酸、碱、盐、活泼金属氧化物、水属于电解质.

练习册系列答案
相关题目
下列有关化学用语等问题中正确的是( )
| A、乙烯的结构简式:CH2CH2 |
B、CH4分子的比例模型: |
C、甲醛分子的电子式: |
D、 2-甲基-3-丁醇 2-甲基-3-丁醇 |
下列溶液中微粒的物质的量浓度关系正确的是( )
| A、室温下,向0.01mol?L-1NH4HSO4溶液中滴加NaOH溶液至中性:c(SO42-)>c(Na+)>c(NH4+)>c(OH-)=c(H+) |
| B、若NaHY的水溶液显碱性,该溶液中粒子浓度关系为:c(Na+)>c(OH-)>c(H+)>c(HY-) |
| C、0.1 mol/L Na2CO3溶液:c(OH-)=c(HCO3-)+c(H+)+2c(H2CO3) |
| D、物质的量都是0.1mol的HCN和NaCN混合后配成1L溶液,c(HCN)+c(CN-)=0.1 mol?L-1 |
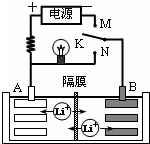 如图是一种可充电的锂离子电池充放电的工作示意图.放电时该电池的电极反应式为:负极:LixC6-xe-=C6+xLi+(LixC6表示锂原子嵌入石墨形成的复合材料)正极:Li1-xMnO2+xLi++xe-=LiMnO2(LiMnO2表示含锂原子的二氧化锰).下列有关说法正确的是( )
如图是一种可充电的锂离子电池充放电的工作示意图.放电时该电池的电极反应式为:负极:LixC6-xe-=C6+xLi+(LixC6表示锂原子嵌入石墨形成的复合材料)正极:Li1-xMnO2+xLi++xe-=LiMnO2(LiMnO2表示含锂原子的二氧化锰).下列有关说法正确的是( )| A、在整个充、放电过程中至少存在3种形式的能量转化 | |||
| B、K与M相接时,A是阴极,发生还原反应 | |||
| C、K与N相接时,Li+由A极区迁移到B极区 | |||
D、该电池的总反应式为Li1-xMnO2+LixC6
|
下列溶液中,溶质的物质的量浓度为1mol?L-1 的是( )
| A、将40 g NaOH溶于1 L 水所得的溶液 |
| B、将0.5 mol?L-1的NaNO3溶液100 mL 加热蒸发掉50 g水所得的溶液 |
| C、将23 g NaCl 溶于水并配成1 L的溶液 |
| D、含K+为2 mol?L-1的K2SO4溶液 |
下面列举了一些化合物的组成或性质,以此能够说明该化合物肯定属于有机物的是( )
| A、仅由碳、氢两种元素组成 |
| B、仅由碳、氢、氧三种元素组成 |
| C、熔点低,且不溶于水 |
| D、在氧气中能燃烧,且只生成二氧化碳 |
化学合成技术对人类健康水平和生活质量的提高做出了巨大贡献.下列各组物质全部为合成高分子材料的是( )
| A、聚乙烯 酚醛树脂 |
| B、麦芽糖 胰岛素 |
| C、淀粉 聚异戊二烯 |
| D、纤维素 涤纶 |
下列关于实验现象的描述不正确的是( )
| A、把锌片和铁片用导线相连,浸入氯化铜溶液,铁片表面出现一层铜 |
| B、把铜片和铁片紧靠在一起浸入稀硫酸中,铜片表面出现气泡 |
| C、把锌粒放入盛有盐酸的试管中,加入几滴氯化铜溶液,气泡放出速率加快 |
| D、把铜片插入三氯化铁溶液中,在铜片表面出现一层铁 |



