题目内容
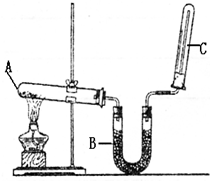
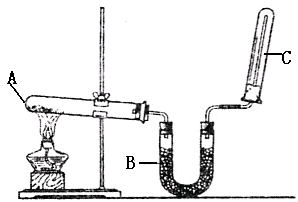
 实验室用图示装置制取乙酸乙酯.
实验室用图示装置制取乙酸乙酯.(1)浓H2SO4的作用是:①
催化剂、
催化剂、
,②吸水剂
吸水剂
.(2)右边试管内装有
饱和碳酸钠溶液;
饱和碳酸钠溶液;
,该溶液的作用是中和乙酸
中和乙酸
、溶解乙醇
溶解乙醇
、降低乙酸乙酯的溶解度.
降低乙酸乙酯的溶解度.
.导气管不能插入液面以下,原因是
防止倒吸
防止倒吸
.加热前,大试管中加入几粒碎瓷片的作用是防止暴沸
防止暴沸
.(3)制取乙酸乙酯的反应方程式是
CH3COOH+C2H5OH
CH3COOC2H5+H2O
| 浓硫酸 |
| 加热 |
CH3COOH+C2H5OH
CH3COOC2H5+H2O
.| 浓硫酸 |
| 加热 |
分析:(1)浓硫酸具有吸水性,脱水性,强氧化性,结合反应即可解答;
(2)饱和碳酸钠溶液与乙酸反应除去乙酸、同时降低乙酸乙酯的溶解度,便于分层;导管伸入液面下可能发生倒吸;液体加热要加碎瓷片,防止暴沸;
(3)酯化反应的本质为酸脱羟基,醇脱氢,该反应生成乙酸乙酯和水,且为可逆反应;
(2)饱和碳酸钠溶液与乙酸反应除去乙酸、同时降低乙酸乙酯的溶解度,便于分层;导管伸入液面下可能发生倒吸;液体加热要加碎瓷片,防止暴沸;
(3)酯化反应的本质为酸脱羟基,醇脱氢,该反应生成乙酸乙酯和水,且为可逆反应;
解答:解:(1)乙酸与乙醇发生酯化反应,需浓硫酸作催化剂,该反应为可逆反应,浓硫酸吸水利于平衡向生成乙酸乙酯方向移动,浓硫酸的作用为催化作用,吸水作用,故答案为:催化剂;吸水剂;
(2)制备乙酸乙酯时常用饱和碳酸钠溶液,目的是中和挥发出来的乙酸,使之转化为乙酸钠溶于水中,便于闻乙酸乙酯的香味;溶解挥发出来的乙醇;降低乙酸乙酯在水中的溶解度,便于分层得到酯;导管不能插入溶液中,导管要插在饱和碳酸钠溶液的液面上,伸入液面下可能发生倒吸;分离乙酸乙酯时先将盛有混合物的试管充分振荡,让饱和碳酸钠溶液中和挥发出来的乙酸,使之转化为乙酸钠溶于水中,溶解挥发出来的乙醇;降低乙酸乙酯在水中的溶解度,静置分层后取上层得乙酸乙酯;液体乙酸乙醇沸点低,加热要加碎瓷片,防止暴沸,
故答案为:饱和碳酸钠溶液;中和乙酸、溶解乙醇、降低乙酸乙酯的溶解度;防止倒吸;防止暴沸;
(3)酯化反应的本质为酸脱羟基,醇脱氢,乙酸与乙醇在浓硫酸作用下加热发生酯化反应生成乙酸乙酯和水,该反应为可逆反应,可为CH3COOH+C2H5OH
CH3COOC2H5+H2O,故答案为:CH3COOH+C2H5OH
CH3COOC2H5+H2O;
(2)制备乙酸乙酯时常用饱和碳酸钠溶液,目的是中和挥发出来的乙酸,使之转化为乙酸钠溶于水中,便于闻乙酸乙酯的香味;溶解挥发出来的乙醇;降低乙酸乙酯在水中的溶解度,便于分层得到酯;导管不能插入溶液中,导管要插在饱和碳酸钠溶液的液面上,伸入液面下可能发生倒吸;分离乙酸乙酯时先将盛有混合物的试管充分振荡,让饱和碳酸钠溶液中和挥发出来的乙酸,使之转化为乙酸钠溶于水中,溶解挥发出来的乙醇;降低乙酸乙酯在水中的溶解度,静置分层后取上层得乙酸乙酯;液体乙酸乙醇沸点低,加热要加碎瓷片,防止暴沸,
故答案为:饱和碳酸钠溶液;中和乙酸、溶解乙醇、降低乙酸乙酯的溶解度;防止倒吸;防止暴沸;
(3)酯化反应的本质为酸脱羟基,醇脱氢,乙酸与乙醇在浓硫酸作用下加热发生酯化反应生成乙酸乙酯和水,该反应为可逆反应,可为CH3COOH+C2H5OH
| 浓硫酸 |
| 加热 |
| 浓硫酸 |
| 加热 |
点评:本题考查了乙酸乙酯的制备,注意把握乙酸乙酯的制备原理和实验方法,把握乙酸乙酯与乙酸、乙醇性质的区别,题目难度不大.

练习册系列答案
相关题目
 实验室用图示装置制取乙酸乙酯.
实验室用图示装置制取乙酸乙酯.
 实验室用图示装置制取干燥的氨气
实验室用图示装置制取干燥的氨气