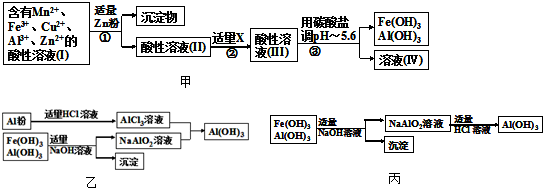
题目内容
 (1)在一定条件下,容积为 100L密闭容器中发生反应:CH4(g)+H2O(g)?CO(g)+3H2(g);△H>0
(1)在一定条件下,容积为 100L密闭容器中发生反应:CH4(g)+H2O(g)?CO(g)+3H2(g);△H>0将1.0mol CH4和2.0mol H2O(g)通入该密闭容器 l0min时有0.1mol CO生成,则10min内该反应的平均速率v(H2)
0.0003mo1?L-1?min-1
0.0003mo1?L-1?min-1
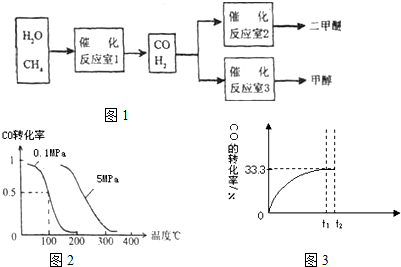
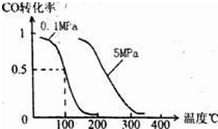
.(2)在压强为0.1MPa条件下,容积为V L某密闭容器中a mol CO与 2a mol H2在催化剂作用下反应生成甲醇:CO(g)+2H2(g)?CH3OH(g);CO的转化率与温度、压强的关系如图所示.
①该反应的△H
<
<
(填“<”、“>”或“=”).②100℃时该反应的平衡常数K=
| v2 |
| a2 |
| v2 |
| a2 |
③在温度容积不变的情况下,向该密闭容器再增加a mol CO与 2a mol H2,达到新平衡时,CO的转化率
增大
增大
(填“增大”、“减小”或“不变”),平衡常数不变
不变
(填“增大”、“减小”或“不变”).分析:(1)根据v=
计算v(CO),再利用速率之比等于化学计量数之比计算v(H2).
(2)①由图可知,压强不变,温度越高CO的转化率越低,故温度升高平衡向逆反应方向移动.
②平衡常数指生成物浓度的系数次幂之积与反应物浓度系数次幂之积的比值,平衡常数k=
,根据CO的转化率,利用三段式计算出平衡时各组分的物质的量,进而求出平衡时各组分的浓度,代入平衡常数计算.
③温度容积不变,向该密闭容器再增加a mol CO与 2a mol H2,等效为开始加入2a mol CO与 4a mol H2,体积扩大1倍,平衡后增大压强,再压缩恢复到原来体积,增大压强平衡向体积减小的方向移动.
平衡常数只受温度影响,温度不变,平衡常数不变.
| △c |
| △t |
(2)①由图可知,压强不变,温度越高CO的转化率越低,故温度升高平衡向逆反应方向移动.
②平衡常数指生成物浓度的系数次幂之积与反应物浓度系数次幂之积的比值,平衡常数k=
| c(CH3OH) |
| c(CO)?c2(H2) |
③温度容积不变,向该密闭容器再增加a mol CO与 2a mol H2,等效为开始加入2a mol CO与 4a mol H2,体积扩大1倍,平衡后增大压强,再压缩恢复到原来体积,增大压强平衡向体积减小的方向移动.
平衡常数只受温度影响,温度不变,平衡常数不变.
解答:解:(1)l0min时有0.1mol CO生成,所以v(CO)=
=0.0001 mo1?L-1?min-1.速率之比等于化学计量数之比,所以v(H2)=3v(CO)=3×0.0001 mo1?L-1?min-1=0.0003 mo1?L-1?min-1.
故答案为:0.0003 mo1?L-1?min-1.
(2)①由图可知,压强不变,温度越高CO的转化率越低,故温度升高平衡向逆反应方向移动,升高温度平衡向吸热反应方向移动,所以正反应为放热反应,即△H<0.
故答案为:<.
②100℃,平衡时CO的转化率为0.5,所以参加反应的CO的物质的量为0.5amol.
对于反应 CO(g)+2H2(g) CH3OH(g);
CH3OH(g);
开始(mol):a 2a 0
变化(mol):0.5a a 0.5a
平衡(mol):0.5a a 0.5a
所以平衡时 CO的浓度为
=
mol/L,H2的浓度为
=
mol/L,CH3OH的浓度为
=
mol/L.
100℃时该反应的平衡常数k=
=
=
.
故答案为:
.
③温度容积不变,向该密闭容器再增加a mol CO与 2a mol H2,等效为开始加入2a mol CO与 4a mol H2,体积扩大1倍,平衡后增大压强,再压缩恢复到原来体积,增大压强平衡向体积减小的方向移动.该反应为气体体积减小的反应,故向正反应移动,CO转化率增大.
平衡常数只受温度影响,温度不变,平衡常数不变.
故答案为:增大;不变.
| ||
| 10min |
故答案为:0.0003 mo1?L-1?min-1.
(2)①由图可知,压强不变,温度越高CO的转化率越低,故温度升高平衡向逆反应方向移动,升高温度平衡向吸热反应方向移动,所以正反应为放热反应,即△H<0.
故答案为:<.
②100℃,平衡时CO的转化率为0.5,所以参加反应的CO的物质的量为0.5amol.
对于反应 CO(g)+2H2(g)
 CH3OH(g);
CH3OH(g);开始(mol):a 2a 0
变化(mol):0.5a a 0.5a
平衡(mol):0.5a a 0.5a
所以平衡时 CO的浓度为
| 0.5amol |
| vL |
| a |
| 2v |
| amol |
| vL |
| a |
| v |
| 0.5amol |
| vL |
| a |
| 2v |
100℃时该反应的平衡常数k=
| c(CH3OH) |
| c(CO)?c2(H2) |
| ||||
|
| v2 |
| a2 |
故答案为:
| v2 |
| a2 |
③温度容积不变,向该密闭容器再增加a mol CO与 2a mol H2,等效为开始加入2a mol CO与 4a mol H2,体积扩大1倍,平衡后增大压强,再压缩恢复到原来体积,增大压强平衡向体积减小的方向移动.该反应为气体体积减小的反应,故向正反应移动,CO转化率增大.
平衡常数只受温度影响,温度不变,平衡常数不变.
故答案为:增大;不变.
点评:考查反应速率、平衡计算与移动、平衡常数等,难度中等,注意③中等效思想的运用.

练习册系列答案
 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案
相关题目