题目内容
根据所学知识判断,下列说法正确的是( )
| A、SO2的水溶液能导电,所以SO2是电解质 | B、酸性溶液里既有H+,又有OH- | C、纯水中c(H+)与c(OH-)的乘积一定等于1×10-14 | D、酸式盐的水溶液一定呈酸性 |
分析:A、SO2的水溶液能导电,但SO2是自身不电离;
B、任何水溶液中都含有H+和OH-;
C、25℃时纯水中c(H+)=c(OH-)=10-7mol/L,c(H+)与c(OH-)的乘积一定等于1×10-14;
D、酸式盐的水溶液的酸碱性取决于酸式根离子的电离程度和水解程度的相对大小.
B、任何水溶液中都含有H+和OH-;
C、25℃时纯水中c(H+)=c(OH-)=10-7mol/L,c(H+)与c(OH-)的乘积一定等于1×10-14;
D、酸式盐的水溶液的酸碱性取决于酸式根离子的电离程度和水解程度的相对大小.
解答:解:A、SO2溶于水后和水反应生成亚硫酸,亚硫酸电离出阴、阳离子而使其溶液导电,电离出阴阳离子的物质是亚硫酸而不是SO2,所以SO2是非电解质,故A错误;
B、酸性溶液里既有H+,又有OH-,且c(H+)>C(OH-),故B正确;
C、25℃时纯水中c(H+)与c(OH-)的乘积一定等于1×10-14,温度升高,平衡正向移动,c(H+)与c(OH-)的乘积增大,故C错误;
D、酸式盐的水溶液,酸式根离子的电离程度小于酸式根离子的水解程度,溶液呈碱性;酸式根离子的电离程度大于酸式根离子的水解程度,溶液呈酸性,故D错误;
故选:B;
B、酸性溶液里既有H+,又有OH-,且c(H+)>C(OH-),故B正确;
C、25℃时纯水中c(H+)与c(OH-)的乘积一定等于1×10-14,温度升高,平衡正向移动,c(H+)与c(OH-)的乘积增大,故C错误;
D、酸式盐的水溶液,酸式根离子的电离程度小于酸式根离子的水解程度,溶液呈碱性;酸式根离子的电离程度大于酸式根离子的水解程度,溶液呈酸性,故D错误;
故选:B;
点评:本题主要考查了电解质、溶液的酸碱性以及水的离子积常数,难度中等,根据所学知识即可完成.

练习册系列答案
 科学实验活动册系列答案
科学实验活动册系列答案
相关题目
 Q、W、X、Y、Z是5种短周期元素,原子序数逐渐增大,Q是周期表中原子半径最小的元素,Q与W组成的化合物是一种温室气体,W与Y、X与Y组成的化合物是机动车排出的大气污染物,Y和Z能形成原子个数比为1:1和1:2的两种离子化合物.
Q、W、X、Y、Z是5种短周期元素,原子序数逐渐增大,Q是周期表中原子半径最小的元素,Q与W组成的化合物是一种温室气体,W与Y、X与Y组成的化合物是机动车排出的大气污染物,Y和Z能形成原子个数比为1:1和1:2的两种离子化合物.
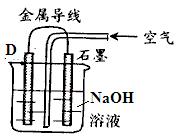 (1)A的元素符号为______,根据所学知识判断,元素114X与B元素是否位于同一主族_______(是或者否),其氯化物的化学式为______________。
(1)A的元素符号为______,根据所学知识判断,元素114X与B元素是否位于同一主族_______(是或者否),其氯化物的化学式为______________。