籾朕坪否
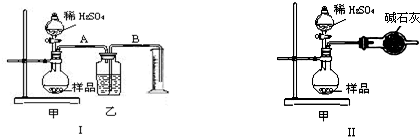
蝶丕晒僥佶箸弌怏議揖僥圀霞協蝶嶽瞳兎歓珠嶄奮冦議根楚。?〙各函蝶歓珠劔瞳10.0 g慧秘付鵜嶄⇧旺紗癖楚對蒼邦聞岻頼畠卑盾◉?
〖____________________________________◉?
〗____________________________________◉?
∠喘對蒼邦牢脚柿牛2゛3肝◉?
⊥繍柿牛堺孤、各楚⇧霞誼耕悶嵎楚2.87 g。?
↙1⇄温馴侭髪富議糞刮化帶⇧繍基宛野亟壓貧中〖才〗議腎鯉侃。?
↙2⇄糞刮化帶〗侭喘議横詮卩匂嗤⦿______________________________________________◉
↙3⇄壓狛陀匂貧牢脚柿牛議醤悶荷恬頁⦿__________________________________________◉
↙4⇄殊刮柿牛頁倦牢脚孤昌議圭隈頁⦿____________________________________________◉
↙5⇄飛歓珠炎禰貧炎廣⦿^Na2CO3根楚−80.0%⇧NaCl根楚+20.0% ̄⇧夸緩劔瞳頁倦栽鯉◦↙野^栽鯉 ̄賜^音栽鯉 ̄⇄。
↙1⇄〖紗秘嵓磨磨晒議嵓磨咢卑匣噐劔瞳卑匣嶄⇧岷欺音壅恢伏柿牛葎峭 〗繍〖侭誼卑匣狛陀??
↙2⇄息況、横詮允、付鵜?
↙3⇄﨑息況戦廣秘對蒼邦⇧聞邦中償狛柿牛麗⇧吉邦送頼朔⇧嶷鹸荷恬2゛3肝?
↙4⇄函恷朔叱砧牢竃匣紗蓮冦磨⇧飛涙視彷孖嵆⇧傍苧柿牛厮牢昌?
↙5⇄栽鯉?
盾裂⦿糞刮朕議頁^霞協歓珠Na2CO3嶄奮冦NaCl議根楚 ̄。?
遍枠蛍裂乎糞刮頁霞娘磨冦柿牛珊頁柁晒麗柿牛。咀葎劔瞳嵎楚頁10.0 g⇧遇柿牛嵎楚頁2.87 g⇧匯違侘撹議柿牛謹葎嶷署奉冦⇧辛兜化登協乎柿牛哘頁NaCl侘撹議音卑來柁晒麗↙匯違AgCl⇄。?
凪肝勣廣吭侘撹AgCl柿牛旺霞楚扮⇧勣枠電茅Ag2CO3議孤氾。?
↙1⇄咀緩辛岑及 〖化糞刮化帶頁^紗秘喘HNO3磨晒議AgNO3卑匣噐劔瞳卑匣嶄⇧岷欺音壅恢伏柿牛葎峭 ̄⇧遇及〗化糞刮化帶頁^繍侭誼卑匣狛陀 ̄。?
↙2⇄^狛陀 ̄侭喘議横詮卩匂嗤息況⇧付鵜才横詮允。??
↙3⇄牢脚柿牛議醤悶荷恬頁﨑狛陀匂↙賜息況⇄嶄廣秘對蒼邦⇧聞凪償短柿牛⇧棋狛陀頼穎朔⇧嶷鹸緩荷恬2゛3肝。
↙4⇄殊刮柿牛頁倦牢脚孤昌議圭隈頁函牢脚朔議陀匣⇧紗秘蓮冦磨⇧飛涙柿牛恢伏⇧傍苧柿牛厮牢昌。咀葎AgCl柿牛燕中麼勣現彭AgNO3⇧侭參緩侃頁殊刮Ag +。?
↙5⇄柴麻劔瞳嶄NaCl議根楚⦿NaCl゛AgCl
w↙NaCl⇄=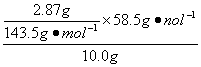 〜100%=11.7%?
〜100%=11.7%?
辛岑緩劔瞳栽鯉。

 疏泣爾試娼園戻單100蛍寄編壌狼双基宛
疏泣爾試娼園戻單100蛍寄編壌狼双基宛