题目内容
8.同温同压下,某气体的密度是氢气密度的8.5倍,现有34g该气体.则:①该气体的物质的量为2mol.
②该气体完全溶解于50mL水后稀释得2L溶液,物质的量浓度1mol•L-1.
分析 同温、同压下是氢气密度的8.5倍,则混合气体的平均相对分子质量为8.5×2=17,结合n=$\frac{m}{M}$计算求解,氨气溶于水溶质是氨气,根据c=$\frac{n}{V}$分析求解.
解答 解:同温、同压下是氢气密度的8.5倍,则混合气体的平均相对分子质量为8.5×2=17,所以摩尔质量为17g/mol,
①该气体的物质的量为:n=$\frac{m}{M}$=$\frac{34g}{17g/mol}$=2mol,故答案为:2;
②该气体完全溶解于50mL水后稀释得2L溶液,c=$\frac{n}{V}$=$\frac{2mol}{2L}$=1mol/L,故答案为:1.
点评 本题考查了分子式的确定,难度不大,把握相对密度与物质的量浓度的计算方法进行推断.

练习册系列答案
相关题目
18.对有机物 的表述不正确的是( )
的表述不正确的是( )
 的表述不正确的是( )
的表述不正确的是( )| A. | 该物质能发生加成、取代、氧化反应 | |
| B. | 该物质遇FeC13溶液显色,lmol该物质遇浓溴水时最多与1mo1Br2发生取代反应 | |
| C. | 该物质的分子式为C11H14O3 | |
| D. | 1mol该物质最多消耗Na,NaOH,NaHC03的物质的量之比为2:2:1 |
16.下列叙述中错误的是( )
| A. | 阿伏加德罗常数的数值与12g 12C所含的碳原子数相等 | |
| B. | 在0.5mol Na2SO4 中,含有的Na+ 数约是6.02×1023 | |
| C. | 等物质的量的O2 与O3,所含氧原子数相等 | |
| D. | 摩尔是物质的量的单位 |
3.CuCl是难溶于水的白色固体,是一种重要的催化剂.工业上,由孔雀石(主要成分Cu(OH)2•CuCO3,含FeS、FeO和SiO2杂质)制备CuCl的某流程如图:
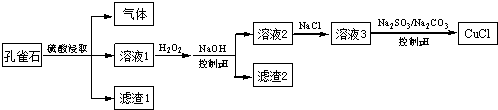
下列说法不正确的是( )

下列说法不正确的是( )
| A. | H2O2将溶液1中Fe2+氧化为Fe3+,再通过控制pH转化为Fe(OH)3除去 | |
| B. | SO32-将溶液3中的Cu2+还原,反应得到CuCl | |
| C. | CO32-作用是控制溶液pH,促使CuCl沉淀的生成 | |
| D. | 若改变试剂加入顺序,将溶液3缓慢加入到含大量SO32-/CO32-的溶液中,同样可制取CuCl |
13.PH=1的盐酸和醋酸分别加水稀释至PH=4,所需水的体积分别为Va、Vb,则( )
| A. | Va=Vb | B. | Va>Vb | C. | Va<Vb | D. | 不能确定 |
 用惰性电极电解200mL一定浓度的硫酸铜溶液,实验装置如图①所示,电解过程中的实验数据如图②所示,横坐标表示电解过程中转移电子的物质的量,纵坐标表示电解过程中产生气体的总体积(标准状况).
用惰性电极电解200mL一定浓度的硫酸铜溶液,实验装置如图①所示,电解过程中的实验数据如图②所示,横坐标表示电解过程中转移电子的物质的量,纵坐标表示电解过程中产生气体的总体积(标准状况).