题目内容
【题目】氮是动植物生长不可缺少的元素,含氮化合物也是重要的化工原料.自然界中存在如下氮的循环过程,工业上也可通过一系列的化学反应模拟该过程,实现氮的转化.
(1)请写出过程①中雷电固氮的化学反应方程式 .
(2)过程③中NH3在土壤中会被微生物转化成HNO2 , 过程④中HNO2会被微生物继续转化为HNO3 , 试写出过程③的化学方程式 .
(3)工业上利用氢气与空气中分离出的氮气合成氨气,模拟实现过程②,写出工业合成氨反应的方程式 .
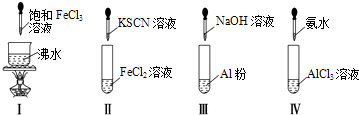
(4)工业上利用氨气制备硝酸.同学甲欲探究硝酸能否与H后金属发生反应,做了如下实验:向盛有稀硝酸的试管中加入Cu片,请你写出相关的实验现象 , 该实验的结论是 .
(5)实验室中用NaNO2与氯化铵共热制取N2 , 该反应体现了NaNO2的性,亚硝酸钠暴露于空气中会生成 , 体现了NaNO2的性. 
【答案】
(1)N2+O2 ![]() 2NO
2NO
(2)2NH3+3O2 ![]() 2HNO2+2H2O
2HNO2+2H2O
(3)N2+3H2![]() 2NH3
2NH3
(4)铜片溶解,溶液变蓝色,生成无色气体在试管口处变红棕色;稀硝酸具有强氧化性,H后金属可以与稀硝酸反应
(5)氧化;NaNO3;还原
【解析】解:(1)放电条件下,氮气和氧气反应生成一氧化氮,反应方程式为:N2+O2 ![]() 2NO,
2NO,
所以答案是:N2+O2 ![]() . 2NO;(2)过程③中NH3在土壤中会被微生物转化成HNO2,2NH3+3O2
. 2NO;(2)过程③中NH3在土壤中会被微生物转化成HNO2,2NH3+3O2 ![]() . 2HNO2+2H2O,
. 2HNO2+2H2O,
所以答案是:2NH3+3O2 ![]() 2HNO2+2H2O;(3)工业合成氨反应的方程式位:N2+3H2
2HNO2+2H2O;(3)工业合成氨反应的方程式位:N2+3H2 ![]() . 2NH3,
. 2NH3,
所以答案是:N2+3H2 ![]() 2NH3;(4)向盛有稀硝酸的试管中加入Cu片,相关的实验现象:铜片溶解,溶液变蓝色,生成无色气体在试管口处变红棕色,该实验的结论是:稀硝酸具有强氧化性,H后金属可以与稀硝酸反应,
2NH3;(4)向盛有稀硝酸的试管中加入Cu片,相关的实验现象:铜片溶解,溶液变蓝色,生成无色气体在试管口处变红棕色,该实验的结论是:稀硝酸具有强氧化性,H后金属可以与稀硝酸反应,
所以答案是:铜片溶解,溶液变蓝色,生成无色气体在试管口处变红棕色;稀硝酸具有强氧化性,H后金属可以与稀硝酸反应;(5)用NH4Cl和NaNO2反应制取N2,反应中NaNO2中+3价N化合价降低,被还原,所以在NaNO2反应中做氧化剂,具有氧化性,亚硝酸钠暴露于空气中会生成硝酸钠,表现亚硝酸钠的还原性,
所以答案是:氧化;NaNO3;还原.

【题目】现有部分短周期元素的性质或原子结构如下表:
元素 | 元素性质或原子的结构 |
T | 2p轨道能级电子数比s能级电子数多1个 |
X | L层p能级电子数比s能级电子数多2个 |
Y | 第三周期元素的简单离子中半径最小 |
Z | L层有3个未成对电子 |
(1)写出元素X的离子结构示意图: . 写出元素Z的简单气态氢化物的电子式:
(2)写出元素Y的最高价氧化物对应的水化物与KOH反应的化学方程式: .
(3)T、Y、Z三种元素的单质中化学性质明显不同于其他单质的是(填元素符号,下同);元素T与氯化素相比,非金属性较强的是 , 下列表述中能证明这一事实的是(填字母).
a.常温下氯气的颜色比T单质的颜色深
b.T的单质通入氯化钠水溶液中不能置换出来
c.氯与T形成化合物中,氯元素呈正价.
【题目】毒重石的主要成分BaCO3(含Ca2+、Mg2+、Fe3+等杂质),实验室利用毒重石制备BaCl22H2O的流程如图: 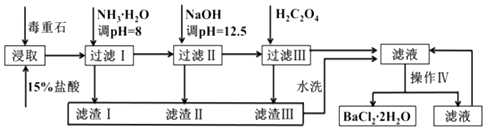
Ca2+ | Mg2+ | Fe3+ | |
开始沉淀的pH | 11.9 | 9.1 | 1.9 |
完全沉淀的pH | 13.9 | 11.1 | 3.2 |
已知:Ksp(BaC2O4)=1.6×10﹣7 , Ksp(CaC2O4)=2.3×10﹣9
(1)实验室用37%的盐酸配制1mol/L盐酸,下列仪器中,不需要使用的是
a.容量瓶 b.量筒 c.烧杯 d.滴定管
为了加快毒重石的酸浸速率,可以采取的措施有(至少两条).
(2)加入氨水调节溶液pH=8的目的是 . 滤渣Ⅱ中含(填化学式).加入H2C2O4时应避免过量,原因是 .
(3)操作Ⅳ的步骤是:、过滤.
(4)利用间接酸碱滴定法可测定Ba2+的含量,实验分两步进行.
已知:2CrO42﹣+2H+=Cr2O72﹣+H2O;Ba2++CrO42﹣=BaCrO4↓
步骤Ⅰ:移取x mL一定浓度的Na2CrO4溶液于锥形瓶中,加入酸碱指示剂,用b molL﹣1盐酸标准液滴定至终点,测得滴加盐酸体积为V0mL.
步骤Ⅱ:移取y mL BaCl2溶液于锥形瓶中,加入x mL与步骤Ⅰ相同浓度的Na2CrO4溶液,待Ba2+完全沉淀后,再加入酸碱指示剂,用b molL﹣1盐酸标准液滴定至终点,测得滴加盐酸的体积为V1mL.通过计算,氯化钡溶液浓度为molL﹣1(用含字母的式子表示).