��Ŀ����
����Ŀ�������йش����С�մ����������ȷ���� �� ��
A. Na2CO3��NaHCO3���������ᷴӦ������������������Һ��Ӧ
B. ������Na2CO3��NaHCO3�ֱ�����ͬŨ�����ᷴӦ��NaHCO3���ĵ����������
C. ��NaHCO3��Һ�е���Ba(OH)2��Һ��������Na2CO3��Һ�м���Ba(OH)2��
Һ���ְ�ɫ����
D. �����ʵ���Na2CO3��NaHCO3�ֱ�������ϡH2SO4��Ӧ��NaHCO3����CO2��
���𰸡�B
��������
A��CO32-+2H+=H2O+CO2����HCO3-+H+=H2O+CO2����HCO3-+OH-=H2O+CO32-����CO32-��NaOH����Ӧ��A����B������������ķ�Ӧ���������ε�����Ϊm g��Na2CO3����HCl ![]() ��NaHCO3��������
��NaHCO3�������� ![]() ��
��![]() ����Na2CO3���ĵ������NaHCO3���࣬����Ũ����ͬʱ��Na2CO3���ĵ������������B��ȷ��C��NaHCO3��Һ�м�������Ba(OH)2ʱ��2NaHCO3+Ba(OH)2=BaCO3��+Na2CO3+2H2O��Na2CO3��Һ�м�������Ba(OH)2ʱ��Na2CO3+Ba(OH)2=BaCO3��+2NaOH��������Ӧ���ܹ����ɰ�ɫ����BaCO3��C����D����A����������ķ�Ӧ���������ε����ʵ�����Ϊ1mol����������ϡ����������ɵ�CO2��Ϊ1mol����������CO2���ʵ�����ͬ��D������ȷ��B��
����Na2CO3���ĵ������NaHCO3���࣬����Ũ����ͬʱ��Na2CO3���ĵ������������B��ȷ��C��NaHCO3��Һ�м�������Ba(OH)2ʱ��2NaHCO3+Ba(OH)2=BaCO3��+Na2CO3+2H2O��Na2CO3��Һ�м�������Ba(OH)2ʱ��Na2CO3+Ba(OH)2=BaCO3��+2NaOH��������Ӧ���ܹ����ɰ�ɫ����BaCO3��C����D����A����������ķ�Ӧ���������ε����ʵ�����Ϊ1mol����������ϡ����������ɵ�CO2��Ϊ1mol����������CO2���ʵ�����ͬ��D������ȷ��B��

 Сѧ��10���ӿ������100��ϵ�д�
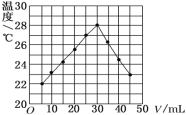
Сѧ��10���ӿ������100��ϵ�д�����Ŀ��������һ�������Դ������CO��ˮ������Ӧ�Ʊ����������仯����ͼ��ʾ��

(1)�÷�ӦΪ���淴Ӧ����800 ��ʱ����CO����ʼŨ��Ϊ2.0 mol��L-1��ˮ��������ʼŨ��Ϊ3.0 mol��L-1���ﵽ��ѧƽ��״̬���CO2��Ũ��Ϊ1.2 mol��L-1����˷�Ӧ��ƽ�ⳣ��Ϊ___�������¶����߸÷�Ӧ�Ļ�ѧƽ�ⳣ���ı仯������___�������������������С��������������
(2)ij�¶��£��÷�Ӧ��ƽ�ⳣ��ΪK=1/9�����¶����ڼס��ҡ������������ܱ�������Ͷ��H2O(g)��CO(g)������ʼŨ�����±���ʾ�������жϲ���ȷ����____(����ĸ)��
��ʼŨ�� | �� | �� | �� |
c(H2O)/mol��L-1 | 0.010 | 0.020 | 0.020 |
c(CO)/mol��L-1 | 0.010 | 0.010 | 0.020 |
A. ��Ӧ��ʼʱ�����еķ�Ӧ������죬���еķ�Ӧ��������
B. ƽ��ʱ�����кͱ���H2O��ת���ʾ���25%
C. ƽ��ʱ������c(CO2)�Ǽ��е�2������0.015 mol��L-1
D. ƽ��ʱ������H2O��ת���ʴ���25%
(3)һ�������£����淴ӦN2(g)+3H2(g)![]() 2NH3(g)����H<0���ﵽƽ���
2NH3(g)����H<0���ﵽƽ���
�ټӴ�����v(��)��v(��)�������仯���ұ仯�ı���__(��������������������)��
����С���ʹ��ϵѹǿ������v(��)___��v(��)___(����������������С������������)��v(��)�仯�ı���__v(��)�仯�ı���(��������������С��������������)��
�۽��£�v(��) ____��v(��)__(����������������С������������)��
���º�ѹ����ͨ��һ������He���ﵽ��ƽ��ʱ��N2��ת����__��c(H2)��__(����������������С������������)��