题目内容
 如图是某学校实验室从化学试剂商店买回来的硫酸试剂标签上的部分内容.据此下列说法正确的是( )
如图是某学校实验室从化学试剂商店买回来的硫酸试剂标签上的部分内容.据此下列说法正确的是( )| A、该试剂的物质的量浓度为18.4 mol?L-1 | B、该硫酸50 mL与足量的铜反应可得到标准状况下SO2 0.46mol | C、要配制200 mL 4.6 mol?L-1的稀硫酸需取该硫酸共50 mL | D、该硫酸与等体积的水混合所得溶液的质量分数小于49% |
分析:A.根据c=
计算;
B.根据Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O及Cu与稀硫酸不反应来分析;
C.根据溶液稀释溶液前后溶质的物质的量不变来计算;
D.水的密度比硫酸的密度小,等体积混合时,硫酸的质量大于水的质量,总质量小于原硫酸溶液的2倍.
| 1000ρw |
| M |
B.根据Cu+2H2SO4(浓)
| ||
C.根据溶液稀释溶液前后溶质的物质的量不变来计算;
D.水的密度比硫酸的密度小,等体积混合时,硫酸的质量大于水的质量,总质量小于原硫酸溶液的2倍.
解答:解:A.c=
=18.4mol/L,故A正确;
B.发生反应Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O,随反应的进行,浓硫酸变为稀硫酸,Cu与稀硫酸不反应,故生成二氧化硫的物质的量小于0.05L×18.4mol/L×0.5=0.46mol,故B错误;
C.根据稀释前后溶质的物质的量不变可知,需取该硫酸的体积为
=0.05L=50mL,故C正确;
D.水的密度比硫酸的密度小,等体积混合时,硫酸的质量大于水的质量,总质量小于原硫酸溶液的2倍,所以该硫酸与等体积的水混合所得溶液的质量分数大于49%,故D错误;
故选AC.
| 1000×1.84×98% |
| 98 |
B.发生反应Cu+2H2SO4(浓)
| ||
C.根据稀释前后溶质的物质的量不变可知,需取该硫酸的体积为
| 0.2L×4.6mol/L |
| 18.4mol/L |
D.水的密度比硫酸的密度小,等体积混合时,硫酸的质量大于水的质量,总质量小于原硫酸溶液的2倍,所以该硫酸与等体积的水混合所得溶液的质量分数大于49%,故D错误;
故选AC.
点评:本题考查溶液物质的量浓度的有关计算,题目难度中等,注意理解掌握物质的量浓度与质量分数的关系,注意硫酸的浓度越大,密度越大.

练习册系列答案
 应用题天天练四川大学出版社系列答案
应用题天天练四川大学出版社系列答案
相关题目
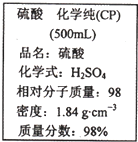 如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.据此下列说法错误的是( )
如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.据此下列说法错误的是( )| A、该硫酸具有强烈的腐蚀性,应放于危险化学用品柜中妥善保管 | B、取10 mL该硫酸于烧杯中,再加等体积的水,可配得49%的硫酸 | C、配制200mL4.6 mol?L-1的稀硫酸需取该硫酸50mL | D、该硫酸与等质量的水混合所得溶液的物质的量浓度小于9.2 mol?L-1 |
 如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.据此,下列说法正确的是( )
如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.据此,下列说法正确的是( )
 如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.据此下列说法不正确的是( )
如图是某学校实验室从化学试剂商店买回的硫酸试剂标签上的部分内容.据此下列说法不正确的是( ) 如图是某学校实验室从化学试剂商店买回的浓硫酸试剂标签上的部分内容.现用该浓硫酸配制100mL 1mol?L-1的稀硫酸.
如图是某学校实验室从化学试剂商店买回的浓硫酸试剂标签上的部分内容.现用该浓硫酸配制100mL 1mol?L-1的稀硫酸.