题目内容
用VSEPR模型预测下列分子或离子的立体结构,其中正确的是( )
| A、NH4+为正四面体形 |
| B、SO2为直线形 |
| C、HCN为平面三角形 |
| D、BF3为三角锥形 |
考点:判断简单分子或离子的构型
专题:化学键与晶体结构
分析:根据价层电子对互斥理论确定微粒的空间构型,价层电子对个数=σ键个数+孤电子对个数,据此分析解答.
解答:
解:A.NH4+中N原子的价层电子对个数=4+
×(5-1-4×1)=4且不含有孤电子对,所以其空间构型为四面体结构,故A正确;
B.SO2分子中价层电子对个数=2+
×(6-2×2)=3且含有1个孤电子对,所以为V形结构,故B错误;
C.HCN的结构为H-C≡N,C原子的价层电子对数为2,不含有孤电子对,为直线形,故C错误;
D.BF3分子中B原子的价层电子对个数=3+
×(3-3×1)=3且不含有孤电子对,所以其空间构型为平面三角形,故D错误;
故选A.
| 1 |
| 2 |
B.SO2分子中价层电子对个数=2+
| 1 |
| 2 |
C.HCN的结构为H-C≡N,C原子的价层电子对数为2,不含有孤电子对,为直线形,故C错误;
D.BF3分子中B原子的价层电子对个数=3+
| 1 |
| 2 |
故选A.
点评:本题考查了微粒空间构型的判断,利用价层电子对互斥理论分析解答即可,难点是孤电子对的计算方法,题目难度不大.

练习册系列答案
相关题目
日本地震导致核电站泄露出大量的人工放射性核素,如131I(碘)、137Cs(铯)等.下列说法正确的是( )
| A、127I与131I为不同的核素,但具有相同的化学性质 |
| B、127I是碘元素稳定的同位素,与131I为互为同分异构体 |
| C、127I与131I的质量数不同,核外电子排布方式也不同 |
| D、铯为IA元素,常温时,0.1mol?L-1的137CsOH溶液,pH<13 |
下列反应中,属于加成反应的是( )
| A、乙烯在空气中燃烧 |
| B、乙烯使酸性高锰酸钾褪色 |
| C、乙炔使溴水褪色 |
| D、苯与液溴反应 |
下列关于油脂的说法正确的是( )
| A、油脂就是脂肪 |
| B、油脂是高分子化合物 |
| C、油脂是混合物 |
| D、油脂都是饱和的 |
下列物质中既含共价键又含离子键的是( )
| A、MgCl2 |
| B、Na2O2 |
| C、K2O |
| D、C6H6 |
 甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是:
甲醇质子交换膜燃料电池中将甲醇蒸气转化为氢气的两种反应原理是:①CH3OH(g)+H2O(g)=CO2(g)+3H2(g);△H=+49.0kJ?mol-1
②CH3OH(g)+
| 1 |
| 2 |
下列说法正确的是( )
| A、反应①中的能量变化如右图所示 | ||
| B、CH3OH转变成H2的过程一定要吸收能量 | ||
| C、根据①推知反应:CH3OH(l)+H2O(g)=CO2(g)+3H2(g)的△H>+49.0kJ?mol-1 | ||
D、根据②推知反应:CH3OH(l)+
|
下列热化学方程式正确的是( )
| A、甲烷的标准燃烧热为890.3 kJ?mol-1,则甲烷燃烧的热化学方程式可表示为:CH4(g)+2O2(g)=CO2(g)+2H2O(g)△H=-890.3 kJ?mol-1 | ||
| B、稀HNO3溶液与NaOH溶液发生反应生成1 mol H2O时放出57.3 kJ的热量.其热化学方程式为:HNO3(l)+NaOH(l)=NaNO3(l)+H2O(l)△H=-57.3 kJ?mol-1 | ||
| C、若:2H2S(g)+O2(g)═2S(s)+2H2O(l)△H=-Q kJ?mol-1.则:2H2S(g)+O2(g)═2S(s)+2H2O(g)△H<-Q kJ?mol-1 | ||
D、若:2CO(g)+O2(g)═2CO2(g)△H=-566 kJ?mol-1;Na2O2(s)+CO2(g)═Na2CO3(s)+
|
某含氧酸的化学式为HnRO2n+2,试判断R的最合理价态为( )
| A、+4 | B、+5 | C、+6 | D、+7 |
下列不属于官能团的是( )
| A、-Br |
| B、OH- |
| C、-CHO |
D、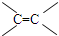 |